МИНИСТЕРСТВО
ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ
АГЕНСТВО ПО ОБРАЗОВАНИЮ
ДАГЕСТАНСКИЙ
ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
Гистологическая ТЕХНИКА
Учебно-методическое пособие
Махачкала
2017
Предметом изучения цитологии, гистологии и эмбриологии являются клеточно-тканевые структуры
организмов на микроскопическом уровне, а предметом изучения – микроскопический
препарат. Поэтому для успешного освоения этих наук необходимо владеть гистологической
техникой – приемами и методами изготовления микроскопических препаратов и способами их изучения. В настоящем
руководстве изложены основные сведения по технике гистологических исследований,
оно знакомит студентов с правилами работы и методами наблюдения под
микроскопом, методикой приготовления препаратов. Особое внимание уделено
методам окрашивания различных клеточно-тканевых структур и гистохимическим
исследованиям. Методики применимы на растительных и животных объектах.
Методические указания
рекомендованы для студентов, специализирующихся по кафедре физиологии человека
и животных, могут быть использованы на лабораторных занятиях по цитологии, гистологии и эмбриологии, большом
практикуме, при выполнении курсовых и дипломных работ.
Автор: Газимагомедова
И.К. – доц. каф. зоологии и физиологии, канд. биол. наук
Содержание
|
1. 1.1. 1.2. 2. 2.1. 2.2. 2.3. 2.4. 2.5. 3. 3.1. 3.2. 3.3. 4. 5. |
Световая микроскопия …………………………………... Устройство
микроскопа…………………………………..... Техника
микроскопирования……………………………… Приготовление постоянного микротомного
препарата Взятие и фиксация
материала ……………………………... Обезвоживание……………………………………………… Уплотнение
(заливка в парафин) …………………………. Приготовление
срезов ……………………………………... Окрашивание
и заключение в бальзам …………………... Методы окрашивания гистологических
препаратов… Общие
методы окраски …………………………...……….. Методы
окраски клеток и неклеточных структур соединительной ткани …………………………………….. Выявление
элементов нервной системы Гистохимические методы исследования......................... Приготовления
препаратов давленных объектов. Методы изучения митоза и мейоза……………………… Литература ………………………………………………….. |
4 4 7 8 8 13 15 16 19 22 23 25 29 30 38 43 |
1. Световая Микроскопия
1.1. Устройство микроскопа
Световой микроскоп является основным прибором
используемым студентами на занятиях. Он имеет следующие основные
характеристики: источник излучения – свет; максимально-полезное увеличение -
х2000-2500; объект – живой и неживой; для окрашивания используют цветные красители; даёт перевернутое, цветное изображение
объекта.
В микроскопе различают оптическую (объектив, окуляр), осветительную
(источник света, зеркало, конденсор и диафрагма) и механическую (штатив, предметный столик, колонка с макро- и
микровинтами, тубус) части (рис. 1).
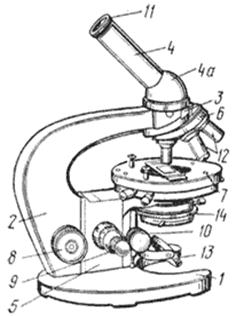
Рис.1. Световой микроскоп.
1 - основание штатива; 2 - колонка штатива; 3 -
головка тубусодержателя; 4 - наклонный тубус; 4а - расширенная часть наклонного
тубуса; 5 - коробка микромеханизма; 6 - револьверная система; 7 - столик
микроскопа; 8 - макрометрический винт; 9- микрометрический винт; 10 - винт
конденсора; 11 - окуляр; 12 - объективы; 13 - зеркало; 14 - конденсор с
ирисовой диафрагмой.
Оптическая
часть. Главная оптическая часть микроскопа - система
линз объектива - обеспечивает увеличение
изображения. Обычные увеличения объектива:![]() 8 ,
8 , ![]() 20 ,
20 , ![]() 40 (сухие
объективы),
40 (сухие
объективы), ![]() 90
(иммерсионный объектив). Окуляр встроен в тубус и позволяет
видеть объект, увеличивая изображение, данное объективом. Используют объективы
90
(иммерсионный объектив). Окуляр встроен в тубус и позволяет
видеть объект, увеличивая изображение, данное объективом. Используют объективы ![]() 5,
5, ![]() 7,
7, ![]() 10,
10, ![]() 15.
15.
Полное увеличение микроскопа оценивают как произведение
увеличений объектива и окуляра, например, при объективе ![]() 20 и окуляре
20 и окуляре
![]() 10 полное
увеличение микроскопа будет
10 полное
увеличение микроскопа будет ![]() 200 (20
200 (20 ![]() 10 = 200
раз).
10 = 200
раз).
Основной характеристикой микроскопа как оптической
системы является разрешающая способность.
Изображения, даваемые объективом, можно увеличить во много раз, применяя
сильный окуляр или, например, путем проекции на экран (до 105 раз).
Разрешающая способность объектива, т.е. минимальное
расстояние между двумя видимыми точками (минимальный размер объекта):
![]()
где:
λ – длина волны света, используемого для освещения объекта; n –
коэффициент преломления среды (воздух или масло); α – угол между
оптической осью объектива и наиболее отклоняющимся лучом, попадающим в объектив
(максимально 90°); n ∙ sin α – апертура линз.
Разрешение микроскопа зависит от длины волны – чем она меньше, тем меньшего
размера деталь мы можем увидеть, – и от апертуры (апертура – функция
светособирающей способности линз, для сухих линз равна 1, а для иммерсионных
линз достигает 1,4), – чем она выше, тем выше разрешение. Обычно в световых
микроскопах используются источники освещения в видимой области спектра (400 – 700
нм), поэтому максимальное разрешение микроскопа в этом случае может быть не
выше 200 - 350 нм (0,2 – 0,35 мкм).
Если использовать ультрафиолетовый свет (260 – 280
нм), то можно повысить разрешение до 130-140 нм (0,13 – 0,14 мкм). Это будет
пределом теоретического разрешения светового микроскопа, определяемым волновой
природой света. Таким образом, все, что может дать световой микроскоп как
вспомогательный прибор к нашему глазу – это повысить разрешающую способность
его примерно в 1000 – 2500 раз. Это и есть “полезное” увеличение микроскопа,
выше которого мы будем только увеличивать контуры изображения, не открывая в
нем новых деталей. Следовательно, при использовании видимой области света 0,2–0,3
мкм является конечным пределом разрешения светового
микроскопа (минимальное расстояние на котором различимы два объекта).
Но все же в световом микроскопе можно видеть частицы
меньшей величины, чем 0,2 мкм. Это метод “темного поля”, или, как его называли раньше, метод
“ультрамикроскопии”. Суть его в том, что, подобно пылинкам в луче света (эффект
Тиндаля), в клетке при боковом освещении светятся мельчайшие частицы (меньше
0,2 мкм), отраженный свет от которых попадает в объектив микроскопа (клетка
выглядит как освещенный объект на темном поле).
Осветительная
часть. Источник света может быть
встроен в микроскоп, а может находиться и вне микроскопа (пример - обычная
настольная лампа).
Зеркало
собирает лучи от источника света и направляет их на препарат снизу. При
искусственном освещении используется вогнутая поверхность зеркала, а при
дневном – плоская.
Конденсор
состоит из линз, которые фокусируют лучи света на препарате. Поднимая и опуская
конденсор (с помощью винта), можно настраивать фокусировку лучей. При подъеме
конденсора попадающие на препарат лучи рассеиваются, при опускании
концентрируются на препарате, но на более ограниченном участке. Обычно работают
при конденсоре, поднятом до уровня столика.
Диафрагма - это система непрозрачных пластинок с
отверстием посередине, которая вмонтирована в конденсор и ограничивает световой
поток, падающий на препарат. При использовании объективов с большим увеличением
отверстие диафрагмы следует уменьшить - для ослабления сферической аберрации.
Механическая
часть. Макро- и микровинты колонки
поднимают и опускают тубус для фокусировки изображения объекта на сетчатке
глаза наблюдателя. Макровинт используется при работе на малом увеличении, а
микровинт - на большом. Предметный столик может перемещаться в горизонтальной
плоскости, что позволяет менять участки препарата, попадающие в поле зрения.
В итоге, световые лучи проходят следующий путь: источник
света → зеркало → конденсор → диафрагма → препарат
→ объектив → тубус → окуляр. Т.е. микроскопия ведётся в
проходящем свете, для чего препарат должен быть достаточно тонким.
1.2. Техника
микроскопирования
Первоначально нужно установить правильное освещение. Поставить
микроскоп от края стола на расстояние не менее
Само изучение препарата начинают с осмотра его глазом,
после чего препарат помещают на предметный столик, покровным стеклом вверх,
прижимая клеммами, чтобы срез точно лег под объектив. Препарат начинают изучать
при малом увеличении, пользуясь макровинтом микроскопа, установить объектив малого
увеличения так, чтобы расстояние между его нижней линзой и покровным стеклом
было равно около 0,5 -
Изучить препарат при малом увеличении.
Перевести препарат на большое
увеличение. Для этого сменяют объектив на ![]() 40
поворотом для револьвера. Медленно и осторожно опускают тубус почти до касания объективом
покровного стекла (до образования узкой щели), чтобы не раздавить стекла.
Медленно вращая микровинт на пол-оборота вперед или назад, достигается четкость изображения. На микровинт бывает
надето кольцо с делениями, показывающими, на сколько микрон мы поднимаем или
опускаем тубус. На левом барабанчике этого винта нанесено 50 делений, и каждое
перемещение на одно деление соответствует 2 микронам. Эти деления также позволяют
оценить толщину препарата и определить, на какой относительной глубине залегают
те или иные структуры в срезе, например, каков слой цитоплазмы над или под
ядром, каков размер последнего.
40
поворотом для револьвера. Медленно и осторожно опускают тубус почти до касания объективом
покровного стекла (до образования узкой щели), чтобы не раздавить стекла.
Медленно вращая микровинт на пол-оборота вперед или назад, достигается четкость изображения. На микровинт бывает
надето кольцо с делениями, показывающими, на сколько микрон мы поднимаем или
опускаем тубус. На левом барабанчике этого винта нанесено 50 делений, и каждое
перемещение на одно деление соответствует 2 микронам. Эти деления также позволяют
оценить толщину препарата и определить, на какой относительной глубине залегают
те или иные структуры в срезе, например, каков слой цитоплазмы над или под
ядром, каков размер последнего.
Для изучения очень мелких структур используют
иммерсионный объектив (![]() 90). При
этом на покровное стекло препарата наносят каплю иммерсионной среды (бывают
масляные, водные, глицериновые), обычно
кедровое масло, затем осторожно опускают тубус до соприкосновения линзы
объектива с маслом. Четкость изображения регулируют микровинтом. После работы
удаляют марлей иммерсионное масло с объектива и покровного стекла.
90). При
этом на покровное стекло препарата наносят каплю иммерсионной среды (бывают
масляные, водные, глицериновые), обычно
кедровое масло, затем осторожно опускают тубус до соприкосновения линзы
объектива с маслом. Четкость изображения регулируют микровинтом. После работы
удаляют марлей иммерсионное масло с объектива и покровного стекла.
2. Приготовление постоянного микротомного препарата
Клетки и ткани можно изучать в живом состоянии путем
изготовления витальных, временных препаратов для однократного изучения, либо
убитые - на соответствующе приготовленных постоянных препаратах, которые
хранятся длительное время.
По характеру взятого материала различают следующие
виды гистологических препаратов: 1) срезы органов (толщиной 5-15 нм), 2)
мазки (крови, костного мозга и т.д.),
3) пленки
(брюшины, мягкой мозговой оболочки), или тотальные препараты. Чаще всего используются срезы.
Приготовление постоянных гистологических препаратов
включает следующие этапы: 1) взятие и фиксация материала; 2) промывка и обезвоживание;
3) уплотнение (заливка в парафин); 4) приготовление срезов; 5) окрашивание; 6)
обезвоживание и заключение препаратов в консервирующую среду (рис. 2).
2.1. Взятие и фиксация материала
Необходимое условие при взятии материала – сохранение
прижизненной организации тканей. Для этого материал берут «живьем» и быстро
убивают, обычно погружая в специальные фиксирующие жидкости, в целях сохранения
витальной структуры, т.е. проводят фиксацию.
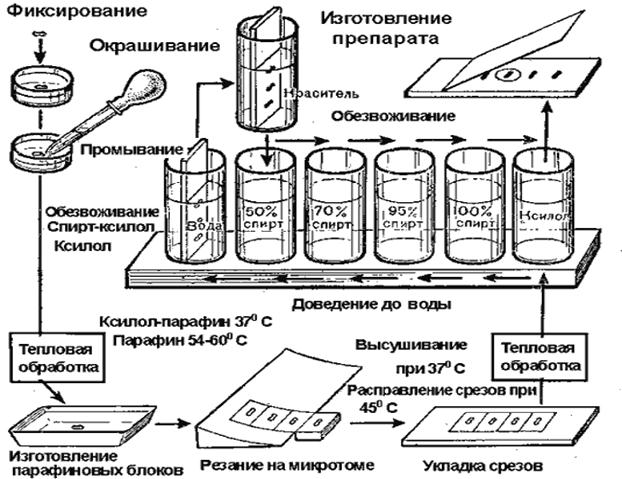
Рис. 2. Этапы приготовления
гистологического препарата для световой микроскопии.
В зависимости от строения органа взятие материала
осуществляется по-разному. Из однородных органов (печень, селезенка) кусочек
можно вырезать из любого участка. Из неоднородных органов (почка, надпочечник)
необходимо так вырезать кусочек, чтобы попали все слои. Величина кусочка
зависит от структуры органа, целей исследования и способов дальнейшей
обработки. Из соответствующего органа вырезают обычно небольшие кусочки (0,5 x 1
x
Фиксация — сохранение картины тканевой структуры изолированных
органов. Задачи фиксации – это убить клетку, остановить активность
внутриклеточных ферментов и распад
клеточных компонентов, стабилизировать макромолекулы путем их химического
сшивания, предотвратить процессы аутолиза (самопереваривания) тканей и их
бактериальное загрязнение, а также избежать потери компонентов клетки или
появления отсутствующих в
живой клетке структур (артефактные
структуры). К сожалению, еще не найден такой химический фиксатор, который бы
удовлетворял всем этим требованиям. Даже наилучшие способы фиксации вызывают
изменения в фиксируемом материале.
Способы фиксации – использование фиксирующих жидкостей, криофиксация
(мгновенное замораживание в жидком азоте) и лиофилизация (замораживание с
последующим высушиванием в вакууме). При лиофилизации выпадает необходимость
проводить обезвоживание и уплотнение материала.
Фиксирующие средства бывают простые и сложные. К
первым относятся спирты, ацетон, кислоты, формалин, сулема, пикриновая кислота,
тетраоксид осмия. Сложными являются смеси различных веществ, например жидкость
Ценкера, жидкость Карнуа, жидкость Буэна и т.д. Так, для лучшей фиксации ядер
употребляют хромовые или хромосмиевые смеси, для фиксации цитоплазмы смеси Карнуа
или Буэна. Фиксирующие свойства зависят от рН среды, температуры,
продолжительности фиксации.
Часто для фиксации клеток используются альдегиды и их
смеси с другими веществами. Широкое применение нашел формалин (формол) в виде
5-15% раствора (продажный формалин - это 35-40% водный раствор формальдегида). Формалин быстро
проникает в ткань, сохраняет структуру объекта, липиды и жиры в тканях. Менее пригодна
фиксация в формалине для ядерных структур. Действие формалина основано на
метилировании тканевых белков: при отщеплении воды формалин вступает с
тканевыми белками в метильное соединение, образуя метиленовые мостики. Т.е.
формалин хорошо связывается с белками, сшивая их с помощью метиленовых
мостиков, вызывая их денатурацию. С липидами формальдегид реагирует слабо (за
исключением фосфатидилэтаноламина). С углеводами альдегиды не реагируют, их
фиксация, сохранность, достигается, по-видимому, за счет стабилизации
окружающих белков.
В последнее время, особенно для электронной
микроскопии, широко используется глютаровый альдегид, который более
эффективно сшивает молекулы и тем самым обладает сильным фиксирующим действием.
В качестве фиксаторов применяют спирты (этанол, метанол),
они значительно больше искажают прижизненную структуру - вызывают необратимую
денатурацию белков, осаждение нуклеиновых кислот и полисахаридов. Осаждающим
действием обладают также сулемовые фиксаторы и фиксаторы с пикриновой
кислотой. Фиксаторы, содержащие тетраоксид осмия (OsО4),
хорошо сохраняют липиды.
Требования, предъявляемые к фиксируемому материалу: 1) свежесть материала, для нормального протекания
жизненных процессов перед фиксацией; 2) небольшие размеры материала - 0,5x1x1
см, для быстрейшего проникновения фиксатора во избежание артефактов. Если
материал нежелательно разрезать на части или он обладает плотной кутикулой и
т.д., то в нескольких местах делают неглубокие надрезы бритвой или проколы
иглой.
Требования, предъявляемые к фиксатору: 1) свежесть; 2) достаточное количество. Объем
фиксатора должен в 20-40 раз превышать объем фиксируемого материала, объект со
всех сторон должен быть окружен фиксатором. Если часть материала плавает на
поверхности фиксатора, то сверху накладывают тонкий слой ваты. Как до, так и
после фиксации объект не должен подсыхать на воздухе.
Приготовление
фиксаторов
Фиксатор
Карнуа:
100%
или 96% спирт……………………6 частей
Хлороформ………………………………3
части
Ледяная
уксусная кислота…………… 1 часть
Фиксатор готовят перед употреблением. Фиксируют от 30
мин до 3 ч, затем кусочки можно хранить в 70% спирте.
Уксусный
алкоголь:
100% или 96% этиловый спирт………...3 части
Ледяная уксусная кислота ..…………….1 часть
Продолжительность
фиксации – 2-12 ч. Иногда в нем хранят материал при 0-3оС.
Фиксатор
Ценкера:
Сулема……………………………………5
г
Двухромовокислый
калий………………2,5 г
Сернокислый
натрий…………………….1 г
Дистиллированная
вода…………………100 мл
Ледяная
уксусная кислота………………5 мл (добавляют перед употреблением)
Фиксируют 1-24 ч. Затем 24 ч промывают
в водопроводной воде до обесцвечивания воды. Материал обесцвечивают в 70% спирте,
где его можно хранить. Цвет фиксатора – насыщенно красно-бордовый. Как только
сулема будет удалена, раствор перестанет обесцвечиваться.
Фиксатор
Батталья:
100%
или 96% спирт…………………….10 мл
Хлороформ……………………………….2
мл
Ледяная
уксусная кислота………………2 мл
Формалин
40%......……………………….2 мл
Фиксируют от 5 мин и более. Фиксатор
пригоден для приготовления временных давленых препаратов.
Формалин:
5%
формалин: 1 часть 40% формалина + 7 частей дистиллированной воды.
10%
формалин: 1 часть 40% формалина + 3 части дистиллированной воды.
20%
формалин: 1 часть 40% формалина + 1 часть дистиллированной воды.
Кусочек ткани помещают в 5% формалин на
1 сут. Перенося в 10% формалин не менее чем на 5-6 сут, где их можно сохранять.
Перед дальнейшей обработкой – обезвоживанием - материал помещают в 20% формалин
на 1 сут. Затем промывают проточной водой 1 сут.
Методика
проведения фиксации. Берется чистая
стеклянная посуда (пробирки, бюксы или стаканчики) с фиксатором, объем которого
в 20-40 раз больше объема материала. На дно посуды кладут гигроскопическую или
стеклянную вату для равномерного пропитывания объекта. Материал с помощью
пинцета быстро помещается в фиксирующую смесь (фиксатор должен быстро проникать
в ткани и не вызывать грубых нарушений тканевых структур) и посуда плотно
закрывается. Вместе с материал в пробирку кладется фиксационная этикетка,
сделанная из плотной бумаги, размером 1х1 см, на которой простым карандашом
отмечаются название изучаемого материала, фиксатора и дата фиксации.
Если ткань богата водой или кровью, фиксатор следует
дважды сменить.
После фиксации образцы промывают проточной водой (в некоторых случаях спиртом) от 1 до
3 ч, иногда дольше. Промывкой материала удаляется излишнее количество
фиксатора. В зависимости от способа фиксации существуют разные способы
промывки. После фиксации в смеси с пикриновой кислотой промывка производится
70-80% спиртом. При фиксации в смесях, содержащих сулему, трихлоруксусную
кислоту, используют 90-96% спирт. При формалиновой фиксации и фиксации
хромовыми смесями промывку производят проточной водой под краном, или
неоднократной сменой воды (10-12 раз) в течение 24-48 ч. Материал,
фиксированный в смесях с преобладанием спирта (фиксатор Карнуа) промывке не
подвергается.
Существуют разные приспособления для промывки: 1) обычные стеклянные склянки с
пробкой или завязанные марлей и резиновым шлангом, соединенные с краном; 2) для
мелких объектов применяются специальные фарфоровые сита; 3) стеклянные
трубочки, обвязанные с обеих сторон марлей.
Удобно провести промывку материала следующим образом:
материал вместе с этикеткой переносят в марлевые узелки, перевязывают их ниткой
и помещают в высокий стакан с водой. Сверху в стакан кладут воронку и все
ставят под кран с проточной водой.
2.2. Обезвоживание
Далее необходимо получить срезы материала для их
последующего окрашивания. Для этого образцы уплотняют, т.е. заливают в парафин
или целлоидин, чтобы в последующем их можно было тонко резать. Предварительно
образцы обезвоживают, чтобы гидрофобный уплотнитель смог проникнуть в ткань.
Обезвоживание производится проведением материала по батарее спиртов
возрастающей концентрации, что позволяет избежать разрывов и деформаций ткани.
Методика
обезвоживания. Материал вынимают из марлевых узелков и вместе с этикеткой
последовательно помещают в стаканчики или бюксы со спиртами (метанол или
этанол) возрастающей концентрации – 70%, 80%, 96%, 100%. Чем нежнее материал,
тем ниже первоначальная концентрация спирта (начинают с 20% спирта). Время
выдерживания в каждом спирте зависит от толщины материала и строения органа: от
30 мин, 1-6 ч, и до 6-12 ч. В 96% и 100% спиртах выдерживают дважды. При
перекладывании материала из слабого раствора спирта в спирт большей
концентрации кусочки необходимо обсушить фильтровальной бумагой.
Схема и сроки выдерживания в спиртах растительного
материала:
|
1.
20% — 30 мин
2.
40% — 30 мин 3.
60% — 30 мин 4.
70-80% — 30 мин (можно оставить на длительное
время) |
5. 96% I —
1 ч 6. 96% II — 1 ч 7. 100% I — 1 ч 8. 100% II — 1 ч |
Схема и сроки выдерживания в спиртах животного
материала, фиксированного в 10% формалине:
|
1.
70% — 8-12 ч 2.
80% — 8-12 ч 3.
96% — 8-12 ч |
4. 100% I — 3-6 ч 5.
100% II — 3-6 ч |
Приготовление
спиртов разной концентрации. Для
получения спиртов 30%, 40%, 50% и т.д. берут соответственно 30, 40, 50 мл 96% спирта
и доводят дистиллированной водой до 96 мл.
Спирты необходимой крепости можно также приготовить готовят
разведением 96% спирта, руководствуясь таблицей:
Таблица
1. Приготовление спиртов
|
Для получения 100мл спирта разного насыщения |
Нужно взять (мл) |
|
|
96% спирта |
воды дистиллированной |
|
|
90% |
93,5 |
6,5 |
|
80% |
83,3 |
16,7 |
|
70% |
72,9 |
27,1 |
|
60% |
62,5 |
37,5 |
|
50% |
52,1 |
47,9 |
|
40% |
41,6 |
58,4 |
|
30% |
31,2 |
68,8 |
Приготовление
абсолютного спирта. Для приготовления абсолютного (100%) спирта используют
безводный медный купорос. Если нет безводного медного купороса, то можно
прокалить в фарфоровой чашке голубые кристаллы СuSО4•5H2O
до белого цвета. На дно банки с притертой крышкой насыпают медный купорос и
заливают 96% спиртом (на 100 мл 96о спирта берут 20-25 мл этого
порошка). Обезвоженная сернокислая медь поглощает остатки воды из спирта и приобретает
голубой цвет. Обезвоживание спирта повторяют несколько раз, пока при заливке
спиртом сернокислая медь не сохранит белый цвет, только тогда спирт станет абсолютным.
2.3. Уплотнение (заливка в парафин)
Существует два способа уплотнения материала:
замораживание образца с последующей резкой на замораживающем микротоме или
пропитывание уплотняющими средами (парафин, целлоидин, желатин, смолы).
Парафин представляет собой смесь разных парафиновых
углеводородов с точкой плавления от 20 до 80о С, для заливки обычно используют
парафин с точкой плавления 52-56оС. Чтобы придать парафину пластичность,
к нему прибавляют 5% пчелиный воск.
Важным условием при заливке в парафин
является полное обезвоживание и удаление спирта, т.к. парафин не растворим в
этаноле. Поэтому перед заливкой необходимо спирт в образце заменить каким-либо
растворителем парафина (ксилолом, толуолом, бензолом, скипидаром, хлороформом и
др.).
Методика
парафинирования. После обезвоживания образцы выдерживают поочередно в
следующих смесях, где вместо ксилола можно использовать хлороформ или толуол:
1.
Этанол 100% + ксилол (1:1) – 6-12 ч.
2.
Чистый ксилол – 6-12 ч.
3.
Парафин + ксилол (1:1), в термостате при 37оС – 6-12 ч.
4.
Парафин I в термостате при 52 - 56оС – 6-12 ч.
5.
Парафин II в термостате при 52 - 56оС – 6-12 ч.
Время выдерживания в каждой среде
приводится для кусочка толщиной 5-
После этого следует заливка в парафин III. В парафинах I и II кусочки можно
проводить много раз. Парафин III готовят про
запас: парафин расплавляют и фильтруют в термостате при 56оС. Затем
парафин смешивают с предварительно отфильтрованным пчелиным воском в
соотношении 6-
Непосредственную заливку пропитанного парафином
материала производят в специальные коробочки, изготовленные из пергамента,
другой плотной бумаги или фольги. Расплавленный чистый парафин разлить в
формочки. Теплым пинцетом переложить пропитанный парафином II кусочек в коробочку, на поверхность слегка застывшего
парафина осторожно кладут этикетку надписью вверх. Парафин должен не менее чем
на 2/3 быть выше уровня кусочка ткани. Коробочку с объектом опускают в широкую
посудину с холодной водой для быстрого застывания парафина. После охлаждения брусочки
парафина с залитым материалом освобождают от бумаги или фольги, получился парафиновый
«пряник». В таком состоянии материал может долго храниться.
2.4. Приготовление
срезов
Срезы толщиной от 3-8 мкм до 1-2 мкм получают с
помощью специального устройства – микротома (рис. 3).
Для получения срезов из парафинового «пряника»
вырезают блок с заключенным образцом и закрепляют на деревянном кубике
(держателе). Блок закрепляется в объектодержатель микротома. При вращении
колеса микротома с помощью микрометрической механической системы
объектодержатель вместе с блоком опускается на нож и перемещается за каждый шаг
на определённое расстояние, оставляя при этом на ноже серийные срезы. Движения
микротомного ножа должны быть быстрыми, отрывистыми.
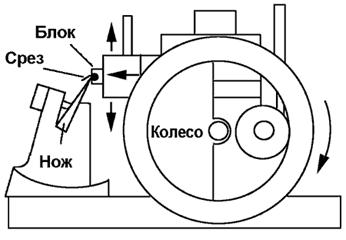
Рис.3. Микротом – устройство для получения гистологических
срезов.
В тех случаях, когда необходимо избежать воздействия
фиксаторов, например при гистохимических методах исследования, используются
микротомы, снабженные специальными охладительными столиками – замораживающие
микротомы. Замороженные срезы переносят в воду или сразу на предметное стекло,
где они оттаивают и расправляются. Метод замораживания значительно ускоряет
приготовление гистологического препарата.
Приготовление
парафинового блока. Из парафинового «пряника»
скальпелем или безопасной бритвой вырезают объект вместе с парафином и
укрепляют его на деревянном кубике (размер около 2 см3). Для этого
на кубик наносят слой расплавленного парафина. Через основание парафинового
блока проводят горячим металлическим предметом (ручкой скальпеля, подогретой на
спиртовке) и опускают его на кубик. После затвердения парафина блок готов для
приготовления срезов. Лишний парафин на блоке нужно отрезать, причем так, чтобы
объект со всех сторон (особенно сверху) был покрыт парафином не менее чем на 1-
Приготовление
срезов на микротоме. Микротом
настраивают, блок устанавливают в объектодержатель, микрометрическим винтом
выбирают необходимую толщину срезов в микронах, микротомный нож устанавливают
под определенным углом наклона к поверхности объекта (13-15о). При
вращении ручки микротома на лезвии ножа будет образовываться прямая лента
срезов парафинового блока.
Полученные срезы снимают с микротомного ножа мягкой
кисточкой, слегка смоченной водой, и переносят на поверхность дистиллированной воды,
нагретой до 40оС для расправления. Срезы кладут той стороной,
которая была обращена к ножу.
Затем на заранее приготовленные чистые и обезжиренные предметные
стекла, на которые наносят каплю белка с глицерином, вылавливают срезы. Для
этого стекло нужно опустить в сосуд, где находятся расплавленные срезы.
Подвести его под срез, подхватить препаровальной иглой срез и удержать в
средней части стекла. Фильтровальной бумагой удалить воду вокруг среза, не
касаясь последнего. Предметное стекло со срезами подписывается простым
карандашом, если оно матировано, или смесью туши с белком.
Срезы сушат в термостате при 37-40оС в
течение 24 ч (иногда 2-3 суток), или оставить при комнатной температуре на более
длительный срок, чтобы не отставали от стекла.
Используют и другие способы расплавления срезов. Для
этого срез наносят на предметное стекло в каплю воды. Затем стекло со срезом
кладут на металлический столик, который нагревают до расплавления срезов (+35оС).
Можно стекло со срезом прямо нагреть над пламенем. После расплавления срезов
остатки воды сливают или удаляют фильтровальной бумагой. Сушат срезы так же,
как и в предыдущем случае.
Парафиновые срезы на предметных стеклах могут длительное
время храниться в коробочках до последующей обработки (окраски).
Приготовление
обезжиренных стекол. Сначала стекла
кипятят в мыльной воде 10-15 мин, затем промывают в холодной проточной воде и
помещают не менее чем на 1 сутки (а лучше на большее время) в насыщенный
раствор К2Сr2О7 в технической серной кислоте – так
называемый «хромпик». Перед приготовлением срезов стекла вынимают из «хромпика»,
очень тщательно промывают в проточной воде и протирают чистой марлей.
Приготовление
смеси белка с глицерином. К свежему
куриному белку добавляют равный объем глицерина. После тщательного взбалтывания
смесь фильтруют и добавляют в нее несколько
кристаллов камфары или тимола для предупреждения загнивания. Каплю полученной
смеси переносят на чистое стекло и растирают пальцем. Стекло можно провести
через пламя для свертывания белка.
Приготовление
туши. Жидкую черную тушь смешивают с
равным объемом куриного белка и глицерина. Делают надпись на стекле и слегка
подогревают надписанный конец.
2.5. Окрашивание и заключение в бальзам
Смысл окраски среза заключается в
усилении светового контраста его различных компонентов, что увеличивает
контрастность структур и делает их более доступными для наблюдения. Окрашивание
представляет собой сложный процесс, в котором соучаствуют физико-химические
факторы субстрата и красителя. Окраска гистологических препаратов определяется
абсорбцией красителю компонентами клеток и связана с электрическими зарядами
красителя и объекта. Большинство применяемых в цитологии красителей представляют
собой водные растворы. По химической характеристике различают красители основные
(катионные), кислые (анионные), нейтральные и индифферентные (табл. 2).
В зависимости от режима работы различают окрашивание прогрессивное,
когда окрашивание объекта доводится до желаемой интенсивности, и регрессивное
окрашивание, при котором ткань в начале заведомо перекрашивается, а затем
избыток красителя отмывается соответствующими реактивами до необходимой
степени. Этот прием основан на неодинаковой прочности связывания красителя с
разными структурами клетки. Извлечение избыточной краски называют дифференцировкой.
Регрессивный метод окраски позволяет получить препараты несравнимо более
высокого качества.
Таблица 2.
Типы красителей
|
Тип красителя |
Пример |
Окрашиваемые
структуры |
|
Кислые |
Кислоты и кислые
соли: эозин, кислый фуксин, пикриновая кислота, флоксин, азокармин,
индигокармин и др. |
Окрашиваемые
структуры основной природы называются оксифильными или ацидофильными (имеющими
сродство к кислым красителям). Это белковые компоненты цитоплазмы, неклеточные
структуры (коллагеновые волокна), некоторые секреторные гранулы. |
|
Основные |
Основные соли: гематоксилин
(точнее, продукт его окисления - гематеин), азур II, кармин, янус зеленый, бисмарк коричневый,
сафронин, пиронин, тионин, альциановый синий и др. |
Красящиеся
структуры кислой природы – базофильные (сродство к основным
красителям). Это структуры, богатые нуклеиновыми или иными кислотами – ядра,
рибосомы; аморфный компонент межклеточного вещества, мукополисахариды, слизь. |
|
Нейтраль-ные |
Смесь двух
красителей: основного (азур II) и кислого (эозин), эозиновый кислый, метиленовый
синий. |
Структуры,
воспринимающие кислые красители, окрасятся эозином; пример - специфические
гранулы в эозинофилах. Ядра всех клеток окрашиваются азуром II. |
|
Индиффе-рентные |
Судан III,
судан IV, осмиевая кислота, шарлах красный. |
Выявляются жиры
и жироподобные вещества. Например, в липидных каплях растворяется судан III. |
Световой микроскоп позволяет видеть не только
фиксированные, но и живые клетки. Для кратковременного наблюдения клетки
помещают просто в жидкую среду на предметное стекло, а для длительного
наблюдения используются специальные камеры. При изучении живых клеток их
окрашивают так называемыми витальными красителями.
Это кислые (трипановый синий, литиевый кармин) или основные красители (нейтральный
красный, метиленовый синий), применяемые при очень большом разведении
(1:200000), следовательно, влияние красителя на жизнедеятельность клетки
минимальное. При окрашивании живых клеток краситель собирается в цитоплазме в
виде гранул, а в поврежденных или мертвых клетках происходит диффузное
окрашивание цитоплазмы и ядра.
Последовательность работы при окрашивании постоянных препаратов:
1. Депарафинирование срезов ксилолом.
2. Удаление ксилола путем замещения его на 100% или 96%
спирт.
3. Удаление спирта промывкой срезов в воде.
4. Окраска и промывка.
5. Обезвоживание срезов в спиртах.
6. Просветление - замещение спирта на ксилол.
7. Заключение в бальзам.
Данная схема может немного отличаться деталями при
различных методах окраски.
Подготовка к
окрашиванию (депарафинирование)
Перед окрашиванием образцы освобождают от парафина,
проводя по батарее растворителей: ксилол, спирт 100%, 96%, 80% 70%, 60%, дистиллированная
вода (по 2-5 мин). Этот ряд кончается водой в том случае, если затем используется
водорастворимый краситель; обводненный препарат легко воспринимает водный
краситель. Теперь срезы готовы к окрашиванию.
Методика
окрашивания. Для окрашивания
предметные стёкла со срезами ставят в маленькие чашки с раствором красителя
попарно, срезами наружу, чтобы каждая пара стеком не соприкасалась. Затем их промывают
водой, обрабатывают раствором другого красителя (если таковой используется) и
вновь промывают водой.
Подробнее различные методы окрашивания препаратов
приводятся далее.
Обезвоживание
и просветление окрашенных срезов
После окрашивания препарат опять обезвоживают (проводя по батарее спиртов с возрастающей
концентрацией – 70%, 96%, 100% по 2-3 мин в каждом).
Затем просветляют в карбоксилоле
(несколько кристаллов карболовой кислоты в ксилоле) и ксилоле по 3-5 мин для
удаления лишней краски.
Карбоксилол, ксилол можно заменить карботолуолом,
толуолом.
Заключение в
консервирующую среду. Ополоснув срезы
дистиллированной водой, можно капнуть сверху глицерин или разогретый раствор
желатина и накрыть покровным стеклом, избегая пузырьков воздуха.
При работе с мазками крови используют кедровое масло.
Большую сохранность и лучшее качество препарата получают,
заключив их в канадский (лучше!) или
пихтовый бальзам.
Заключение в бальзам. Растворяют канадский бальзам в ксилоле (толуоле) до
консистенции жидкого меда. Растворение идет медленно. Каплю такого раствора быстро,
пока не испарился ксилол (толуол), наносится на покровное стекло и оно быстро накрывается
над срезом. Можно капать бальзам на предметное стекло на поверхность среза и
быстро покрывать его покровным стеклом. Канадский бальзам должен полностью
покрыть срез. Следят, чтобы не было пузырей воздуха. Через 1-2 дня бальзам застывает.
Заключение в глицерин-желатин. Растворяют
3. МЕТОДЫ ОКРАШИВАНИЯ
ГИСТОЛОГИЧЕСКИХ ПРЕПАРАТОВ
Существует большое количество различных способов
окраски, представим лишь наиболее употребляемые. Общими, наиболее
распространенными методами являются окраска железным гематоксилином (по
Генденгайну) и окраска гематоксилин-эозином.
3.1. Общие методы окраски
Окраска железным гематоксилином (по
Генденгайну)
Метод удобен тем, что пригоден после любого фиксатора,
как для зоологических, так и ботанических объектов, для изучения и ядерных, и
плазменных структур, межклеточных образований, мышечных волокон.
Гематоксилин – это эфирная вытяжка кампешевого дерева,
в сухом виде имеющая вид бесцветных кристаллов. Само по себе это вещество не
является красителем, а становиться таковым после окисления (кислородом воздуха
или добавлением NaIO3) и превращения в гематеин.
Препарат предварительно обрабатывают (протравляют)
железоаммиачными квасцами, а потом окрашивают гематоксилином. Структуры
приобретают коричневато-серый, почти черный цвет.
Приготовление
красителя.
Так в течение 3-4 недель гематоксилин окислится до
гематеина, цвет его из светло-желтого станет вишнево-коричневым. В хорошо закрытом
сосуде краситель годен в течение длительного времени.
Методика
1. Удаляют парафин ксилолом – 15 мин.
2. Удаляют из срезов ксилол 96% спиртом – 20 мин.
3. Гидратируют срезы в двух порциях дистиллированной воды
по 5 мин.
4. Срезы протравливают железоаммиачными квасцами 4% в
течение 6-24 ч, в зависимости от их толщины, затем ополаскивают в
дистиллированной воде в течение 5-10 мин.
5. Окрашивают гематоксилином 0,5% - 6-24 ч.
6. Ополаскивают в дистиллированной воде – 1 мин.
7. Проводят дифференцировку под микроскопом железоаммиачными
квасцами.
8. Промывают срезы водой – 15-20 мин.
9. Обезвоживают в спиртах (70%, 96%, 100%) по 2-3 мин в
каждом.
10.
Просветляют в
карбоксилоле и ксилоле – по 3-5 мин (в ксилоле можно дольше).
11.
Заключают в
бальзам.
Окраска гематоксилин–эозином
Это самый распространённый метод окраски; сочетание
основного и кислого красителей позволяет выявить почти все клетки и многие
неклеточные структуры. Ядра приобретают сине-фиолетовый цвет, цитоплазма -
желтовато-розовый цвет.
Примечание: используемый гематоксилин готовится по
методу Эрлиха: окисляется до гематеина калийными квасцами.
Приготовление
красителей
Гематоксилин:
Раствор должен созреть в течение 2 недель в сосуде,
прикрытом бумажным колпачком, при частом взбалтывании, пока не примет
темно-красный цвет.
Эозин (0,1%
раствор): 10 мг эозина растворить в 100 мл дистиллированной воды.
Методика
1. Удаляют парафин ксилолом – 15 мин.
2. Удаляют из срезов ксилол 96% спиртом – 20 мин.
3. Гидратируют срезы в двух порциях дистиллированной воды
по 5 мин.
4. Окрашивают гематоксилином в течение 2-3 мин.
5. Ополаскивают в дистиллированной воде – 5-10
мин.
6. Окрашивают в водном растворе эозина
0,1% - 1-2 мин. Для лучшего окрашивания можно продлить время окраски или
подкислить раствор эозина каплей 3% уксусной кислоты.
7.
Промывают в дистиллированной воде –
0.5-1 мин.
8. Обезвоживают в спиртах (70%, 96%,
100%) по 2-3 мин в каждом.
9. Просветляют в карбоксилоле и ксилоле – по 2-3
мин.
10.
Заключают в бальзам.
3.2.
Методы окраски клеток и неклеточных структур соединительной ткани
Окраска по Романовскому
(Гимза)
Метод
используют для окрашивания мазков крови.
Раствор
Романовского содержит метилен-азур, метиленовый фиолетовый, метиленовый синий и
эозин. Смесь основных и кислых красителей дает различное окрашивание клеточных
элементов. Ядра красно-фиолетовые. Эозинофилы красновато-коричневые.
Базофильные гранулы синие. Нейтрофильные гранулы красно-фиолетовые. Эритроциты
бледно-красные. Цитоплазма лейкоцитов (лимфоцитов) голубая или синяя.
Приготовление
мазков крови. Взяв предметное стекло
за длинные края, прикасаются его поверхностью (отступя 0,5-
Хорошо сделанный мазок тонок, имеет желтоватый цвет и
оканчивается «метелочкой».
Мазки быстро сушат на воздухе, т.к. при медленном
высыхании изменяется морфология клеток.
Приготовление
основного раствора красителя. В
продаже имеется готовый раствор красителя, а также сухая краска Романовского
(Гимзы), из которой готовят раствор:
Колбу подогревают на водяной бане или в термостате при
60оС, часто взбалтывая. Остудив, фильтруют через сухой фильтр в
чистую бутыль их темного стекла и плотно закрывают резиновой пробкой. Можно
длительно хранить.
Разбавление
основного раствора. В химический
стакан отмеряют 10 мл прокипяченной дистиллированной воды, приливают каплями из
градуированной пипетки 0,3 мл основного раствора и слегка покачивают (не
встряхивать!).
Если краситель сразу после разбавления выпадает в
осадок, то раствор не годен к употреблению, т.к. окрашивающая способность теряется. Причина в нечистой посуде, плохой
дистиллированной воде или старом основном растворе.
Фиксация. Свежие, высушенные на воздухе препараты фиксируют в
метиловом спирте 5-10 мин или в абсолютном спирте, или в спирт-эфире 30 мин.
Методика. Предметные стекла обсушивают и помещают (мазком вверх)
горизонтально в чашку Петри на параллельные стеклянные палочки. Раствор краски
разбавляют и сразу наливают на мазки. Окрашивать 30-45 мин, после чего мазки
вынуть и хорошо промыть дистиллированной водой, обсушить на воздухе. В случае
перекраски дифференцируют в воде.
Мазки можно заключить в кедровое или парафиновое
масло.
Окраска азур-эозином по Нохт-Максимову
Цитоплазма окрашивается в оттенки синего цвета, базихроматин
- в темно-синий, оксихроматин - розовый, соединительная ткань – нежно-розовый
цвет.
Приготовление
красителей. Готовят два основных
раствора, которые могут храниться несколько месяцев в плотно закрытой темной
посуде.
Раствор А:
Фиксация.
Используют смесь Ценкера, спирт-формалин или абсолютный спирт.
Методика. Срезы из прокипяченной дистиллированной воды помещают
на 6–12–24 ч в раствор красителя; в течение этого времени не должен появляться
грубый хлопьевидный осадок. При перекрашивании срезы дифференцируют в 96%
спирте до появления красной окраски в эритроцитах. Обезвоживают в абсолютном
спирте в течение 30-60 сек.
Далее – 3 порции чистого ксилола, нейтральный бальзам
или кедровое масло.
Окраска тканей гематоксилином-пикрофуксином
по Ван-Гисону
Обычно данный метод рекомендуется для окрашивания неклеточных
структур соединительной ткани. Эта окраска дает прекрасные сочные обзорные
трехцветные препараты.
Коллагеновые волокна соединительной ткани окрашивается
в ярко-красный цвет, эластические волокна – в желтый цвет, мышечная и остальные
ткани - в различные оттенки буроватого и желто-зеленого, ядра - в черный цвет
(резко выделяясь на желто-красном фоне).
Приготовление
красителей. Гематоксилин здесь
рекомендуется брать в прописи Вейгерта, так как в этом случае ядра более
контрастно видны на желто-красном фоне.
Гематоксилин Вейгерта получают путем смешивания двух растворов. Раствор I представляет собой 1% раствор гематоксилина в 96%
этиловом спирте, раствор II – смесь 4 мл раствора полуторахлористого железа, 1 мл
25% соляной кислоты и 95 мл дистиллированной воды. Оба раствора (I и II) смешивают в
равной пропорции и получают темно-фиолетовую смесь.
Пикрофуксин готовят
предварительно. Он состоит из насыщенного при комнатной температуре водного
раствора пикриновой кислоты (ее надо взять 100 мл) и 10 мл 1% водного раствора
кислого фуксина.
Методика. Срезы красят 2-5 мин смесью гематоксилина Вейгерта,
затем переносят в проточную воду, после чего докрашивают пикрофуксином 1-2 мин.
Окончательную обработку окраски производят под
контролем микроскопа, дифференцируя до желательной интенсивности слабым (около
40%) этиловым спиртом или сперва водой, а потом более крепким (до 96%) спиртом. Окраску завершают
отмыванием препарата проточной водой.
Окраска по Маллори
Краситель является трёхцветным: это смесь кислого
фуксина, анилинового синего, оранжевого, а также двух кислот. Коллогеновые волокна соединительной ткани и
ретикулярная соединительная ткань окрашиваются в темно-синий цвет, многие другие структуры (ядра, мышечные волокна,
эритроциты) - в оранжевый или красный цвет, хроматин - красный до желтовато-коричневого тона, слизь
– синий цвет.
Приготовление
красителей
0,1% раствор кислого фуксина:
1% раствор фосфорно-молибденовой кислоты:
Раствор А:
Фиксация удается красивее всего после фиксации в сулеме или
жидкости Ценкера. Сносные результаты и после фиксации формалином.
Методика. Окрашивают в 0,1% кислом фуксине – 3 мин.
Промывают в воде и фиксируют окраску 1%
фосфорно-молибденовой кислотой – 3-5 мин.
Промывают в воде и окрашивают в растворе А – 2 мин.
Промывают в воде, дифференцируют в 96% спирте; затем –
абсолютный спирт, ксилол, бальзам.
Окраска орсеином
Рекомендуется для окрашивания эластических
волокон. В настоящее время широко применяется также для окраски хромосом в
изолированных клетках, например в культурах ткани.
Эластические волокна соединительной ткани окрашиваются
в темно-красный цвет, а остальные
структуры – в слабо-розовый.
Приготовление
красителя. 1% раствор орсеина в 70%
этиловом спирте (
Методика. Срезы выдерживают в красителе в течение 1 ч.
Затем их ополаскивают в дистиллированной воде,
обезвоживают в спиртах и дифференцируют под контролем микроскопа.
3.3. Выявление элементов нервной системы
Импрегнация нервной системы нитритом
серебра
Уплотнение образца осуществляют не путём заливки в
парафин (или целлюлозу), а путем замораживания. Срез готовят на замораживающем
микротоме. Всю обработку срезов ведут в химически чистой посуде.
При окрашивании срез последовательно обрабатывают
растворами азотнокислого серебра, формалина, аммиачного серебра. В результате
окрашивания элементы нервной системы (волокна, клетки и т.д.) окрашиваются в
чёрный цвет, а окружающие ткани – в светло-коричневый цвет.
Приготовление
красителя
Раствор азотнокислого серебра: готовят 20% раствор азотнокислого серебра на
бидистиллированной воде, которая не дает мути с серебром (
Помутневший, а тем более побуревший раствор негоден.
Перед импрегнацией раствор азотнокислого серебра переводят в аммиачное серебро:
в чашечку с 5 мл 20% раствора азотнокислого серебра по каплям добавляют 25%
аммиак, причем выпадает черный осадок, который растворяется при дальнейшем
добавлении аммиака. Как только осадок исчезнет, добавление аммиака прекращают.
Аммиачная вода: растворяют 1 часть 25% аммиака в 2 частях дистиллированной воды.
20% формалин: 1 часть 40% формалина + 1 часть дистиллированной воды.
Фиксации. Фиксируют кусочки в нейтральном 15-20% формалине в течение длительного
времени – не менее 7 суток.
Методика. Срезы
помещают на 2-15 мин в 20% раствор азотнокислого серебра.
Затем на стеклянной палочке проводят, не опуская на
дно чашки, через 3-4 порции 20% раствора формалина. Фильтровальной бумагой
удаляют избыточную жидкость и погружают срезы в аммиачное серебро.
Контролируя под микроскопом, выжидают выявления в
срезе элементов нервной ткани, принимающих черную окраску. Импрегнацию
продолжать до отчетливого проявления нервных структур.
Из аммиачного серебра срезы переносят в аммиачную воду
на 10-15 мин, где импрегнация прекращается.
Срезы промывают в нескольких порциях дистиллированной
воды, обезвоживают и заключают в бальзам.
4. Гистохимические
методы исследования
Цито- и гистохимические методы основаны на специфической реакции между химическим
реактивом и определённым компонентом препарата, позволяют выявить различные
химические соединения в структурах
клеток и тканей и их локализацию. Образующийся продукт реакции имеет окраску,
отличную от окраски исходного реактива.
В основе этих методов лежат избирательное окрашивание
(в реакцию с красителем вступают определенные химические группировки клеточных
веществ); избирательное растворение красителя в определенном субстрате клетки;
образование в ходе промежуточных реакций неокрашенного продукта, с последующим
переводом его в окрашенный; активизация химических веществ, неспособных
взаимодействовать с красителем.
Целая группа цито- и гистохимических реакций связана с
обнаружением ферментов. Общий принцип этих реакций в том, что в микроскоп видны
не сами белковые ферменты, а места их локализации, которые обнаруживаются по
продуктам специфической ферментативной активности. Для этого необходимо брать
клетки с сохранившейся активностью фермента. В этом случае используют
специальные щадящие методы химической фиксации или же методы замораживания
объектов для того, чтобы можно было сделать срезы с твердых замороженных блоков
тканей. Чтобы обнаружить активность фермента, клетки помещают в среду,
содержащую субстрат для данной ферментативной реакции и реагенты, связывающиеся
специфически с конечными продуктами реакции. Конечные продукты не должны
мигрировать с места реакции и, что тоже очень важно, должны давать окрашивание.
Примером такой ферментативной гистохимической реакции может быть реакция на
выявление фосфатазы – фермента, отщепляющего фосфатную группу от
фосфоорганических соединений (фосфомоноэстераза).
Выявление ДНК реакцией Фельгена
Основной реактив – фуксинсернистая кислота (реактив
Шиффа). Реакция основана на том, что дезоксирибоза молекулы ДНК в ходе
гидролиза с соляной кислотой превращается в альдегид, который при
взаимодействии с фуксинсернистой кислотой окрашивается в красно-фиолетовый
(пурпурно-красный) цвет. Таким образом,
реакция Фельгена состоит из двух этапов: гидролиза и окрашивания.
В качестве контроля используются препараты, не
подвергавшиеся гидролизу. Их помещают в реактив Шиффа на 10-15 мин. Окрашивания
не должно быть.
Приготовление
растворов
Реактив Шиффа:
Сернистая вода (раствор метабисульфита натрия или калия): к 100 мл проточной воды
добавляют 5 мл 10% метабисульфита и 5 мл 1 н НСI. Используют в работе только свежий раствор.
Методика
1. Срезы депарафинируют ксилолом – 15 мин.
2. Удаляют из срезов ксилол 96% спиртом – 15 мин.
3. Гидратируют срезы в дистиллированной воде – 5-10 мин.
4. Быстро споласкивают в холодной 1 н НСI и помещают
в 1 н НСI для гидролиза при 60оС – 8 мин.
5. Быстро споласкивают в холодной 1 н НСI, затем в дистиллированной воде.
6. Окрашивают реактивом Шиффа – 0,5- 1 ч.
7. Срезы осушают и споласкивают в трех порция раствора
сернистой воды по 2-3 мин в каждой.
8. Споласкивают в дистиллированной воде – 5 мин.
9. Обезвоживают в спиртах (70%, 96%, 100%) по 2-3 мин в каждом.
10. Просветляют в двух порциях ксилола – 10 и 5 мин.
11. Заключают в бальзам.
Выявление РНК и ДНК методом Браше
Используется для одновременного выявления ДНК и РНК.
Реактив - смесь двух красителей: метилового зелёного и
пиронина. Метиловый зеленый окрашивает ДНК хромосом в зеленый цвет, а пиронин
окрашивает РНК ядрышек и цитоплазмы в красный цвет.
Приготовление
красителя
Необходимо предварительно очистить метиловый зеленый
от примесей метилового фиолетового, который всегда содержится в красителе. Для
этого встряхивают водный раствор красителя с избытком хлороформа или амилового
спирта (они растворяют метиловый фиолетовый). Водный верхний слой затем
отделяют для дальнейшего применения (желательно после 2-3 дней стояния).
Раствор метилового зеленого–пиронина. Рекомендуется применять пиронин G или Y.
Раствор состоит из 17,5 мл 5% водного раствора
пиронина, 10 мл 2% водного раствора метилового зеленого (промытого в
хлороформе) и 250 мл дистиллированной воды.
Фиксация смесью Карнуа.
Методика
1. Срезы освобождают от
парафина ксилолом – 15 мин.
2. Удаляют из срезов ксилол 96% спиртом – 15 мин.
3. Гидратируют срезы в дистиллированной воде – 5-10 мин.
4. Окрашивают раствором метилового зеленого–пиронина – 10
мин.
5. Промывают в дистиллированной воде в течение нескольких
секунд (иначе вымывается пиронин).
6. Досуха промокают фильтровальной бумагой.
7. Обезвоживают в абсолютном ацетоне – 2-3 мин.
8. Споласкивают в смеси, состоящей из равных частей
ацетона и ксилола, в 10% растворе ацетона в ксилоле.
9. Просветляют в двух порциях ксилола – 10 и 5 мин.
10.
Заключают в
бальзам.
Выявление полисахаридов Шифф-йодной
кислотой – ШИК (по Мак-Манусу)
Йодная кислота – окислитель – разрывает
С–С–связи в веществах, содержащих две смежные гликолевые группы в положении 1,
2 (СНОН–СНОН), превращая такие соединения в диальдегид (СНО–СНО). Диальдегид
взаимодействует с реактивом Шиффа с образованием нового соединения, которое
имеет красный цвет. Таким образом, углеводы окрашиваются в различные оттенки
пурпурно-красного цвета, гликоген окрашивается в более темный цвет.
Приготовление
реактивов
0,5% раствор йодной кислоты НIО4 или ее соли КIО4:
Реактив Шиффа (см. методику «Выявление ДНК реакцией Фельгена»).
Целестиновый голубой:
Гемалаун Майера:
Фиксация смесью
Карнуа, можно и другие.
Методика
1. Срезы освобождают от
парафина ксилолом – 15 мин.
2. Удаляют из срезов ксилол 96% спиртом – 15 мин.
3. Гидратируют срезы в дистиллированной воде – 5-10 мин.
4. Окисляют 0,5% раствором НIО4 или КIО4 – не более 2-5 мин.
5. Промывают в дистиллированной воде.
6. Окрашивают реактивом Шиффа – 10-15 мин.
7. Промывают в проточной воде в течение 5-10 мин.
8. Докрашивают ядра сначала целестиновым голубым, затем
гемалауном Майера по 2-3 мин в каждом растворе.
9. Срезы дифференцируют в 1% подкисленном спирте (1%
солянокислый).
10.
Промывают в
проточной воде – 30 мин.
11.
Обезвоживают в
спиртах (проводить очень быстро!).
12.
Просветляют в ксилоле
– 5-10 мин.
13.
Заключают в
бальзам.
Выявление белка реакцией Милона
(модификация Бэкера)
Белки, содержащие тирозин, окрашиваются
в красный, розовый или оранжево-красный цвет.
Фиксация.
Формалин, парафиновые срезы.
Приготовление
реактива.
Методика. Срезы проводят через 50% спирт до воды. Помещают в
небольшой сосуд, содержащий реактив, и осторожно нагревают до кипения.
Прекратив нагревание, дают остыть до комнатной температуры. Срезы вынимают из
раствора и промывают в трех порциях дистиллированной воды (по 2 мл в каждой
порции).
Заключают в глицерин-желатин. Обезвоживают,
просветляют и заключают в консервирующую среду.
Выявление
жира суданом III
Выявление липидов основано на способности нейтральных
жиров окрашиваться растворенными в них красителями, например cуданом III. Капли жира окрашиваются
в яркий оранжево-красный цвет.
Фиксация формалином.
Приготовление
красителя. В колбе смешивают 0,2-
Методика. При приготовлении препарате не используют какие-либо
растворители жира (спирты, ксилол и др.). Срезы режут на замораживающем
микротоме; из воды срезы переносят в глицерин, минуя растворители жира.
Для окрашивания жира срез помещают в краску cудан III на несколько
минут. Затем дополнительно окрашивают гематоксилином (см. методику «Окраска
гематоксилин-эозином») и заключают его в капле глицерина под покровное стекло.
Во избежание высыхания края покровного стекла заливают расправленным парафином
или воском.
Выявление кислой фосфатазы методом
азосечения
Здесь в качестве субстрата используется
α-нафтилфосфат, который расщепляется кислой фосфатазой до α-нафтола,
вступающего в реакцию сочетания с солью диазония. В результате участки,
обладающие ферментативной активностью, окрашиваются в красновато-коричневый
цвет. При более длительной инкубации в местах локализации фосфатазы наблюдается
образование кристаллов: выпадают осадки конечного продукта реакции темно-синего
цвета.
Приготовление
реактивов
α-нафтилфосфат: нагревают с обратным холодильником
Инкубационная смесь α-нафтилфосфата: 10-20 мг α-нафтилфосфата растворяют в 20 мл
молярного вероналацетатного буфера (Михаэлис) при рН 5, добавляют
Фиксация. Тонкие (2-
Методика. Нарезают замороженные
срезы толщиной 10-15 мкм, наклеивают их на стекла без какого-либо клеящегося
вещества. Подсушивают при комнатной температуре в течение 2-3 ч, чтобы срезы
хорошо приклеились.
Далее срезы инкубируют при 37оС в смеси с α-нафтилфосфатом
в течение 30-60 мин для печени крысы: смесь хорошо встряхивают и
отфильтровывают непосредственно на подсушенные срезы. Промывают в проточной
воде – 2 мин. Заключают в глицерин-желатин.
Хорошие результаты дают препараты, нарезанные в
криостате, нефиксированных тканей и свободно плавающих в инкубационной смеси (с
инкубацией в течение 15-30 мин).
Выявление сульфгидрильных групп
по Шевремону и Фредерику
Реакцию можно проводить как на свежих, так и на
фиксированных мазках и срезах.
На присутствие сульфгидрильных групп указывают синие
гранулы или тонкий коллоидный осадок, похожий на диффузную синюю окраску. Фон
желтоватый. Препараты сохраняются длительное время.
Фиксация. Кусочки ткани толщиной 3-
После фиксации промывают не в воде, а в
50% спирте или в формалине с раствором Рингера.
Приготовление
реактивов
0,8%
раствора NaCI:
Раствор Рингера:
Реактив А (готовят
и профильтровывают непосредственно перед употреблением): 1 часть свежего 0,1%
раствора железосинеродистого калия и 3 частей 1% раствора сульфата железа Fe(SO4)3, рН 2,4.
Смесь на свету может сохраняться около 2 ч, она не
должна соприкасаться с металлическими предметами.
Методика. Готовят тонкие парафиновые или замороженные срезы. В
промежуточных средах и парафине выдерживают как можно меньше времени.
Срезы депарафинируют и тщательно споласкивают
дистиллированной водой. Помещают в три порции реактива А на 20 мин. Долее
следует длительная промывка в проточной воде и заключение бальзам.
Пероксидазная реакция (по Лизону)
Употребляют стабильный лейкокислотный
фуксин, восстановленный цинковой пылью с уксусной кислотой, который дает очень
ясные, стойкие препараты. Гранулы пероксидазы окрашиваются в синий цвет.
Метод применяют для материала,
фиксированного формалином, или мазков крови, фиксированных формалином или 70%
спиртом.
Приготовление
раствора. Смешивают
Перед употреблением отфильтровывают 10
мл раствора и прибавляют 1 мл обычной перекиси водорода.
Методика.
Срезы окрашивают под контролем 5-10 мин. Затем промывают, окрашивают
каким-либо гистологическим методом и заключают через спирты в бальзам.
Для мазков крови реактив разбавляют в 5-10 раз.
5.
ПРИГОТОВЛЕНИЕ ПРЕПАРАТОВ ДАВЛЕННЫХ ОБЪЕКТОВ. МЕТОДЫ
ИЗУЧЕНИЯ МИТОЗА И МЕЙОЗА
Давленные препараты не требуют для своего
приготовления сложных процедур обезвоживания, парафинирования и приготовления
микротомных срезов. Их используют при изучении митоза, мейоза, кариотипов,
хромосомных нарушений, анализе пыльцы и др.
Наиболее часто для изготовления давленных препаратов
используют фиксаторы Карнуа, уксусный алкоголь, Батталья. Часто применяют
специальную обработку материала перед фиксацией колхицином 0,01-0,2% (в
зависимости от объекта) в течение 2-5 ч. При действии колхицина хромосомы укорачиваются,
происходит накопление метафаз, что делает хромосомы более наглядными.
Окрашивают препараты ацетокармином, ацетоорсеином,
ацетолакмоидом, реактивом Шиффа.
Хорошие объекты для изучения митоза – корешки
проросших семян лука, бобов, гороха; для изучения мейоза – рожь, лук,
традесканция, семенники животных.
Общая схема работы:
1. Фиксируют материал в течение нескольких часов в
уксусном алкоголе или смеси Карнуа.
2. Промывают материал в 70% спирте до исчезновения запаха
уксусной кислоты.
3. Хранят материал в 70% спирте.
4. Промывают материал в воде.
5. Материал помещают для мацерации в 1 н соляную кислоту
при 60оС на несколько минут или секунд (в зависимости от объекта).
6. Промывают объект в воде.
7. Материал помещают в краситель на несколько минут
(необходимо подогревание на спиртовке, не доводя до кипения).
8. Для размягчения тканей объект кладут на предметное
стекло в каплю 45% уксусной кислоты или хлоралгидрата (
Приготовление
красителей
Ацетокармин: смешивают 45 мл ледяной уксусной кислоты, 55 мл дистиллированной воды
и от 0,5 до
Другой способ:
Порошок кармина добавляют в кипящую жидкость
небольшими порциями с тем, чтобы предотвратить выброс красителя с парами из
колбы.
Ацетоорсеин:
Ацетолакмоид:
Приготовление временного давленного
препарата слюнных желез дрозофилы
С помощью данного препарата можно ознакомиться с
микроскопическим строением гигантских, политенных хромосом дрозофилы.
1. Под бинокулярной лупой с помощью препаровальных иголок выделяют слюнные железы в каплю
физраствора.
Слюнные железы расположены по обе
стороны пищевода в переднем отделе тела.
2. Переносят железы иглой в уксусный алкоголь для
фиксации – 15 мин.
3. Окрашивают ацетокармином – 20 мин.
Для ускорения окрашивание можно
проводить в термостате при 37оС.
4. Окрашенную железу переносят глазной пипеткой на
обезжиренное предметное стекло в каплю 45% уксусной кислоты или хлоралгидрата.
Кислоту меняют, «отсасывая» ее фильтровальной бумагой.
5. Объект осторожно накрывают покровным стеклом, не
занося пузырьков воздуха. Поверх покровного стекла кладут фильтровальную
бумагу, давят пальцем на покровное стекло; выступающую из-под него уксусную
кислоту, промокают фильтровальной бумагой.
Круговыми движениями тупого конца
препаровальной иглы давят железы под покровным стеклом, стекло при этом не
должно сдвигаться (поэтому края покровного стекла хорошо обсушивают).
6. Покровное стекло по краю заливают узкой кромкой
парафина или клея БФ-2, пользуясь скальпелем. Временный препарат готов.
Приготовление давленного препарата из
молодых листочков
Для изучения митозов удобно
использовать временные давленные препараты из молодых листочков.
1. Проводят фиксацию молодых листочков (размер 2-
2. Мацерация в смеси соляной кислоты и спирта (1:1) в
течение 0,5 -1ч.
3. Промывают дистиллированной водой – 5-10 мин.
4. Окрашивают ацетокармином или ацетолакмоидом в тигельке
или пробирке при нагревании, несколько раз доводя до кипения – 3-5 мин.
5. Окрашенные листочки помещают в 45% уксусную кислоту на
предметное стекло. Отделяют от листочка его основание, где чаще встречаются
митозы, а остальную часть удаляют. Основание листочка раздавливают под
покровным стеклом, и препарат рассматривают под микроскопом.
Перевод
временных препаратов в постоянные. Продлить
время хранения временных препаратов до года, иногда и более позволяет использование
различных замазок и заключающих сред. Замазками смазывают края покровного
стекла тонкой стеклянной палочкой,
предварительно осушив препарат фильтровальной бумагой или 3-5 мин в сушильном
шкафу при 37-39оС.
В качестве замазки используют:
1. Клей БФ-2.
2.
Заключающие среды:
1. 10% раствор глицерина в 45% уксусной кислоте.
2. Лактофенол: смешивают при нагревании
Существует еще такой метод перевода временного
препарата в постоянный: препарат ставят на лед; когда покровное стекло
отскочит, снимают его и капают бальзам и снова покрывают покровным стеклом
(предварительно лучше обезводить).
Метод отпечатков при исследовании мейоза
у животных
Этим методом удобно изучать различные
фазы мейоза.
Вскрывают семенник, производя надрез,
пинцетом берут свежий кусочек ткани. Ткань прикладывают надрезом несколько раз
к предметному стеклу в разных местах, оставляя мутные пятнышки, где и будет
находиться клетки с мейозом.
Проводят фиксацию смесью Карнуа в
течение 10-15 мин. Стекла извлекают из фиксатора, дают обсохнуть и наносят
каплю ацетокармина. Накрывают покровным стеклом и смотрят под микроскопом.
Препарат можно перевести в постоянный:
после высыхания предметного стекла и обсушки покровного стекла препарат
опускают в ксилол, затем в бальзам.
Если препарат «грязный», его окунают в
10% уксусную кислоту и проводят через батарею спиртов или ацетоксилольной
смеси: чистый ацетон, ацетон+ксилол (1:1), чистый ксилол и еще раз чистый
ксилол.
ЛИТЕРАТУРА
1. Андерс А.Г. Пособие для практических занятий по
гистологии и общей эмбриологии. Учеб пособие для студентов пед. ин-тов. - М.,
Просвещение, 1969. - 168 с.
2.
Бумагина С.И.
Цитогенетика. Методические указания к практическим занятиям. – Махачкала, ИПЦ
ДГУ, 1982. - 28 с.
3.
Волкова О.В.,
Елецкий Ю.К. Основы гистологии с гистологической техников. – М.: Медицина,
1982.
4.
Гистология / Под
ред. Ю.И.Афанасьева и Н.А.Юриной. - М.: Медицина, 1999. – 374 с.
5.
Кухтина Ж.М.
Руководство к практическим занятиям по цитологии. Учеб. Пособие для естеств.
фак-тов пед. ин-тов. - М., Просвещение, 1971. - 111 с.
6.
Лабораторные
занятия по курсу гистологии, цитологии и эмбриологии: Учеб. Пособие для мед.
вузов/ Ю.И.Афанасьев, Л.П.Бобова, В.Л.Горячкина и др.; Под ред. Ю.И.Афнасьева,
А.Н.Яцковского. – М.: Медицина, 1999. – 328 с.
7.
Справочник по
клиническим лабораторным методам исследования / Н.И.Бокуняева, Ю.С.Жевелик,
Р.П.Золотницкая и др.; Под ред. Е.А.Кост. – М.: Медицина, 1975. – 384 с.
Афанасьев
Ю.И., Н. А. Юрина, Е. Ф. Котовский и др. Гистология, эмбриология, цитология Москва, 2012. - 800 с.
2.
Гемонов В.В., Лаврова Э.Н. Гистология, цитология и эмбриология. Москва, 2012. -
168с.
3.
Атлас гистологии / Под ред. В.В. Банина.
– М., 2011. - 264с.
4.
Кузнецов С.Л., Мушкамбаров Н.Н.
Гистология, цитология, эмбриология (краткий курс). –М., 2014. - 175 с.
Изабела Курбанмагомедовна Газимагомедова
Гистологическая техника
Учебно-методическое
пособие
_______________________________________________________________