Тема
3. КРОВЬ И ЛИМФА. КРОВЕТВОРЕНИЕ
План:
2. Структурно-функциональная
характеристика форменных элементов крови.
3. Особенности
формулы крови у детей.
1. Состав и функции крови
Кровь и лимфа, являющиеся соединительными тканями, которые образуют внутреннюю
среду организма, состоят из плазмы (жидкого межклеточного вещества) и
взвешенных в ней форменных элементов. Обе ткани тесно взаимосвязаны, в
них происходит постоянный обмен форменными элементами, а также веществами,
находящимися в плазме. Например, рециркуляция лимфоцитов из крови в лимфу и из
лимфы в кровь; из плазмы крови образуется тканевая жидкость, а из тканевой
жидкости в лимфатических сосудах образуется лимфа.
Система крови включает в себя следующие
компоненты:
1) кровь и лимфу;
2) органы кроветворения и иммунопоэза;
3) клетки крови, выселившиеся из крови в
соединительную и эпителиальную ткани и способные вернуться (рециркулировать) снова в
кровеносное русло (лимфоциты).
Состав крови (рис. 13):
1) форменные элементы – 40-45%;
2) плазма - жидкое межклеточное
вещество – 55-60%.
В связи с тем, что в крови содержатся как истинные
клетки (лейкоциты), так и постклеточные образования (эритроциты и тромбоциты), в совокупности их принято
именовать их форменными элементами.
Плазма
крови состоит из:
1) неорганические
вещества: воды (90-92%)
и 1% минеральных солей (из них 0,9% – NaCl.
2) органические вещества (7–9%): белки – 7-8%, липиды – 0,7-0,8%,
углеводы (глюкоза) – 0,12%, мочевина – 0,03% и др).
В
плазме содержатся белки, аминокислоты, нуклеотиды, глюкоза, минеральные
вещества, продукты обмена: мочевина, мочевая кислота, креатинин, билирубин и
т.д. Функция плазмы –
транспорт растворимых веществ.
Белки плазмы крови:
1) альбумины;
2) глобулины (в том числе
иммуноглобулины);
3) протромбин, фибриноген (свертывающие
белки);
4)
антитромбин, фибринолизин (антисвертывающие);
5)
белки ферменты и др.
Гемограмма или формула крови взрослого человека
отражает количественное содержание форменных элементов:
1) эритроцитов содержится:
а) у мужчин
– 3,9–5,5×1012 /л, или
3,9–5,5 млн/мл3, концентрация
гемоглобина130–160 г/л;
б) у женщин – 3,7–4,9×1012/л, гемоглобин – 120–150 г/л;
2) тромбоцитов – 200–300×109/л;
3) лейкоцитов – 3,8–9×109 /л (т.
е. в 1000 раз меньше, чем эритроцитов). 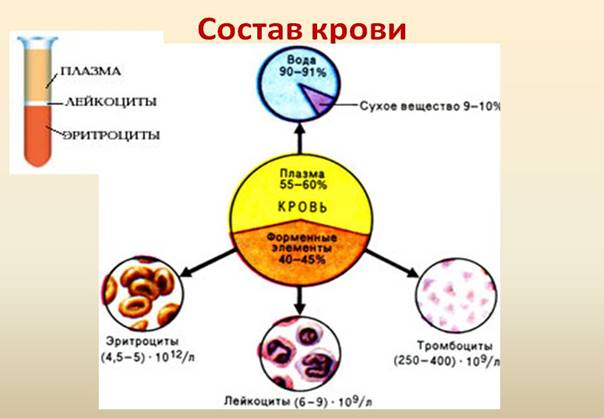
Рис. 13. Состав крови.
Функции крови:
1) транспортная: перенос газов (за счет способности
гемоглобина связывать кислород и углекислый газ), различных питательных и
биологически активных веществ;
2)
трофическая: после расщепления
питательных веществ в процессе пищеварения мономеры всасываются и переносятся
кровью к клеткам всех органов и тканей;
3)
дыхательная:
кровь участвует в газообмене в легких (внешнее дыхание) и тканях (тканевое
дыхание) за счет транспорта кислорода и углекислого газа;
4) иммунная или защитная: неспецифическая защита (система
комплемента, фагоциты, NK клетки) и специфическая (Т и В
лимфоциты) иммунная защита;
5) экскреторная или
выделительная: кровь приносит к почкам продукты обмена (мочевина, креатинин,
билирубин, соли), которые затем выводятся с мочой.
6) терморегуляторная: перераспределение тепла в организме.
7) гомеостатическая:
все эти функции обеспечивают гомеостаз или постоянство внутренней среды
организма.
2.
Структурно-функциональная характеристика
форменных элементов крови
2.1. Эритроциты – красные кровяные тельца, преобладающая популяция форменных элементов
крови, высокодифференцированные
постклеточные структуры, неспособные к делению.
Функции
эритроцитов:
1) дыхательная или транспорт
газов – O2 и СО2;
2) транспорт аминокислот, антител, гормонов,
токсинов, ряда лекарственных веществ,
адсорбируя их на поверхности плазмолеммы.
Популяция
эритроцитов неоднородна по форме и размерам.
Форма эритроцитов:
1) двояковогнутые диски – дискоциты (80%);
2) остальные 20% – сфероциты, планоциты, эхиноциты,
седловидные, двуямочные.
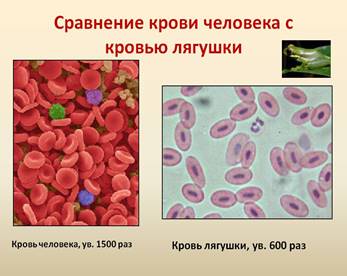
Рис.14.
Кровь человека и лягушки.
По размеру выделяют
следующие виды эритроцитов:
1) нормоциты (7,1-7,9 мкм, концентрация нормоцитов в периферической крови –
75%);
2) макроциты (размером более
8 мкм, количество – 12,5%);
3) микроциты (размером менее
6 мкм – 12,5%).
Обязательной составной частью популяции эритроцитов являются их молодые формы (1-5 % от общего числа) –ретикулоциты или полихроматофильные эритроциты. В них сохраняются рибосомы и эндоплазматическая сеть.
Процесс старения эритроцитов идет двумя путями –
кренированием (образование зубцов на плазмолемме) или путем инвагинации
участков плазмолеммы (рис. 15).
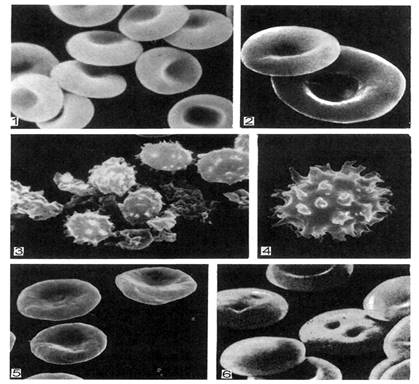
Рис. 15. Эритроциты
человека различной формы в сканирующем электронном микроскопе, × 8000 (по
Г.Н.Никитиной).
1
- дискоциты-нормоциты (80-90 %); 2 – дискоцит; 3,4 – эхиноциты; 5 -
стоматоциты; 6 - сфероцит (2-6 - стареющие формы).
Цитоплазма эритроцита
состоит из воды (60%) и сухого остатка (40%), содержащего около 95% гемоглобина
и 5% других веществ.
Гемоглобин – основной белок цитоплазмы эритроцита. Количество гемоглобина в одном эритроците называют цветным
показателем.
Гемоглобин
– это сложный белок, обладающий высокой способностью связывать кислород. Он
состоит из 4 полипептидных цепей глобина и гема (железосодержащий порфирин), В
норме у человека содержится два типа гемоглобина – HbА
и HbF, которые отлтчаются составом аминокислот в белковой части.
У взрослого человека преобладает НbА –
98%, включающие 574 аминокислоты, а HbF – 2%. У новорожденных –
фетальный гемоглобин (от англ, foetus – плод) HbF – 80%, а НbА –
20%.
Железо (Fe2+)
+ О2 = оксигемоглобин (HbO2),
железо (Fe2+)
+ СО2 = карбогемоглобин (HbСO2),
железо (Fe2+)
+ СО = карбоксигемоглобин (HbСO) –
это стойкое
соединение, его накопление в крови ведет к смерти от удушья в результате
развития гипоксии или кислородного голодания.
В легких образуется оксигемоглобин, который
транспортируется ко всем органам и тканям и там отдает О2.
В тканях он превращается в карбоксигемоглобин (рис. 16). При разрушении
эритроцитов (токсины, радиация и др.) гемоглобин выходит из клеток, и это
явление называется гемолизом. При заболеваниях могут появляться аномальные
формы эритроцитов, что чаще всего обусловлено изменением структуры гемоглобина
(Hb). Замена даже одной аминокислоты в молекуле Hb может быть причиной
изменения формы эритроцитов. Процесс нарушения формы эритроцитов при
заболеваниях получил название пойкилоцитоз.

Рис. 16. Дыхательная функция крови.
Также в плазмолемме эритроцита – 15 белков с молекулярной
массой 15-250 КД. Спектрин -
примембранный белок цитоскелета,
связанный с цитоплазматической стороной плазмолеммы, участвует в поддержании
двояковогнутой формы эритроцита. Мембранные белки – гликофорин и полоса
3. Гликофорины – рецепторные белки, обнаружены только в
эритроцитах. Полоса 3 – гликопротеид участвует в обмене О2 и СО2. Эритроциты в легких отдают СО2 путем замены анионов НСО3-
на Cl-, а белок полоса 3 обеспечивает этим анионам трансмембранный
проход через гидрофильные "поры" (водные ионные каналы).
По содержанию на мемране
эритроцитов агглютиногенов А и В и в плазме α- и β-агтлютининов
различают 4 группы крови. При переливании крови для предотвращения гемолиза
(разрушение эритроцитов) нельзя допускать вливания реципиентам эритроцитов с
агглютиногенами А или В, имеющим α- или β-агглютинины.
Поэтому лица с 0(I) группой крови являются универсальными донорами, а лица с
АВ(IV) группой крови являются универсальными реципиентами, т.е. им можно
перелить любую группу крови.
На поверхности эритроцитов имеется также резус-фактор (Rh-фактор) – агглютиноген. Он присутствует у 86%
людей; у 14% отсутствует (резус-отрицательные).
Переливание резус-положительной крови резус-отрицательному пациенту вызывает
образование резус-антител и гемолиз эритроцитов.
Агглютинация – склеивание эритроцитов, которые
образуют при этом так называемые "монетные столбики" (рис. 17). Это
явление связано с потерей заряда плазмолеммы эритроцитов, так как в движущейся
крови эритроциты отталкиваются из-за наличия на их плазмолемме одноименных
отрицательных зарядов. Скорость оседания (агглютинации) эритроцитов (СОЭ) в 1 ч
у здорового человека составляет 4-8 мм у мужчин и 7-10 мм у женщин. СОЭ служит
важным диагностическим признаком, при многих
заболеваниях ускоряется СОЭ, например, при воспалительных процессах.
Живут эритроциты
– 120-130 дней. Ежедневно в организме
разрушается около 200 млн. эритроцитов. Главным образом старые эритроциты
разрушаются макрофагами в селезенке, а также в печени и костном мозге, при этом
гемоглобин распадается, а высвобождающееся из гема железо используется для
образования новых эритроцитов. В макрофагах гемоглобин
распадается на пигмент билирубин и гемосидерин –
агрегаты, содержащие железо. Железо гемосидерина связывается с трансферрином – негеминовым белком плазмы, содержащим железо, и захватывается
специальными макрофагами костного мозга. В процессе образования эритроцитов
(эритропоэз) эти макрофаги передают трансферрин в формирующиеся эритроциты, что
послужило основанием назвать их клетками-кормилками.
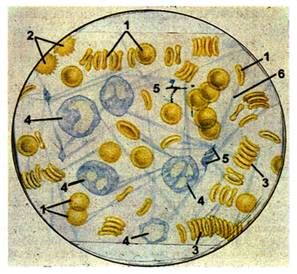
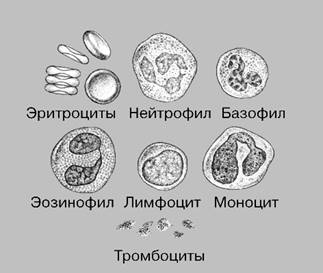
Рис. 17. Кровь: 1 -
эритроциты (дискоциты); 2 - эритроциты с выростами цитоплазмы (эхиноциты); 3 -
"монетные" столбики эритроцитов (агглютинировавшие эритроциты); 4 -
лейкоциты; 5 -тромбоциты (кровяные пластинки); 6 - нити фибрина.
Число эритроцитов у здоровых
людей может меняться в зависимости от возраста, эмоциональной и мышечной
нагрузки, экологических факторов и др.
Возрастные изменения красной крови:
Число эритроцитов в момент рождения и в первые часы жизни
выше, чем у взрослого человека, и достигает 6,0-7,0×1012/л. К
10-14 сут оно равно тем же цифрам, что и во взрослом организме. В последующие
сроки происходит снижение числа эритроцитов с минимальными показателями на
3-6-ем месяце жизни (физиологическая анемия). Число эритроцитов становится
таким же, как и во взрослом организме, в период полового созревания. Для
новорожденных характерно наличие анизоцитоза (разнообразие размеров) с
преобладанием макроцитов, увеличенное содержание ретикулоцитов, а также присутствие
незначительного числа ядросодержащих предшественников эритроцитов.
2.2.
Тромбоциты (или
кровяные пластинки) – фрагменты цитоплазмы крупных клеток красного костного мозга (мегакариоцитов)
округлой, овальной, отростчатой формы, не имеющие ядра и многих органоидов,
размером 2-4 мкм. Молодые
формы тромбоцитов крупнее старых. Продолжительность жизни – 5-8 дней.
Составные части тромбоцита:
1) гиаломер (основа
пластинки, окруженная плазмолеммой);
2) грануломер (зернистость, представленная
специфическими гранулами, а также фрагментами зернистой ЭПС, рибосомами,
митохондриями и др.) (рис. 18).
Функция тромбоцитов – участие в свертывании крови путем образования тромба.
При
повреждении стенок сосудов тромбоциты разрушаются, и один из важных факторов свертывания выходит
в плазму и способствует превращению растворимого белка фибриногена в
нерастворимые нити фибрина (они основа тромба).
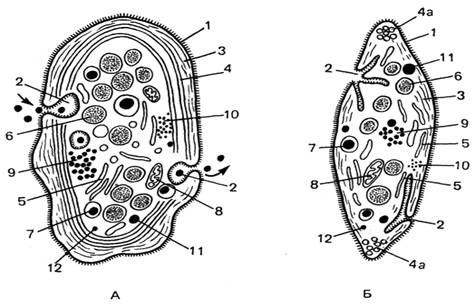
Рис. 18. Ультрамикроскопическое
строение тромбоцита (кровяной пластинки) (по Н.А.Юриной). А - горизонтальный
срез; Б - поперечный срез. 1 - плазмолемма с гликокаликсом; 2 -открытая система
каналов, связанная с инвагинациями плазмолеммы; 3 - актиновые филаменты; 4 -
циркулярные пучки микротрубочек; 4а - микротрубочки в поперечном разрезе; 5 -
плотная тубулярная система; 6 - α-гранулы; 7 - β-гранулы; 8 -
митохондрии; 9 -гранулы гликогена; 10 - гранулы ферритина; 11 - лизосомы; 12 -
пероксисомы.
В тромбоцитах содержится около 12 факторов,
участвующих в свертывании крови. Остановка кровотечения
(гемостаз) включает 3 основные фазы изменений:
1) освобождение активного
тромбопластина из тромбоцитов (внутренний фактор) и из тканей сосуда (внешний
фактор) в зоне поврежденной сосудистой стенки;
2) образование под влиянием
тромбопластина из неактивного протромбина активного тромбина;
3) под влиянием тромбина из
фибриногена образуется нерастворимый фибрин. Фибрин формирует нити толщиной 25
нм. Для всех фаз свертывания крови необходим Са2+.
Затем, в сгусток, состоящий в основном из тромбоцитов
и фибрина, проникают фибробласты и капилляры и происходят замещение сгустка
соединительной тканью и его ретракция, связанная с сокращением
нитей актина в отростках тромбоцитов и нитей фибрина. Рассасывание тромба
(фибринолиз) происходит под влиянием ферментов антисвертывающих систем крови. В
гиаломере кровяных пластинок, помимо актина, содержится фактор ретракции
кровяного сгустка. При ретракции сгустка сокращается
его объем до 10 % от первоначального, изменяется форма пластинок (дисковидная
становится шаровидной), наблюдаются разрушение пограничного пучка
микротрубочек, полимеризация актина, появление многочисленных миозиновых филаментов,
формирование актомиозиновых комплексов, обеспечивающих сокращение сгустка.
Отростки активированных пластинок вступают в контакт с нитями фибрина и
втягивают их в центр тромба.
В организме существуют и
противосвертывающие системы. Известно, что мощным антикоагулянтом является
гепарин, вырабатываемый тучными клетками. Уменьшение свертывания крови
отмечаются при ряде заболеваний.
Усиление свертывания крови обусловливает образование тромбов в кровеносных сосудах, например при атеросклерозе, когда изменены рельеф и целостность эндотелия. Уменьшение числа тромбоцитов (тромбоцитопения) приводит к снижению свертываемости крови и кровотечения. При наследственном заболевании гемофилии имеют место дефицит и нарушение образования фибрина из фибриногена. При заболеваниях соотношение различных форм тромбоцитов может изменяться, что учитывается при постановке диагноза. Повышение количества юных форм наблюдается у новорожденных. При онкологических заболеваниях увеличивается число старых тромбоцитов.
Важной функцией тромбоцитов является их участие в
метаболизме серотонина. Тромбоциты – это практически единственные элементы
крови, в которых из плазмы накапливаются резервы серотонина. Связывание
тромбоцитами серотонина происходит с помощью высокомолекулярных факторов плазмы
крови и двухвалентных катионов с участием АТФ.
В процессе свертывания крови из
разрушающихся тромбоцитов высвобождается серотонин, который действует на
сосудистую проницаемость и сокращение гладкомышечных клеток сосудов. Серотонин
и продукты его метаболизма обладают противоопухолевым и радиозащитным
действием. Торможение связывания серотонина тромбоцитами обнаружено при ряде
заболеваний крови – злокачественном малокровии, тромбоцитопенической пурпуре,
миелозах и др.
Продолжительность жизни тромбоцитов - в среднем 9-10
дней. Стареющие тромбоциты фагоцитируются макрофагами селезенки. Усиление
разрушающей функции селезенки может быть причиной значительного снижения числа
тромбоцитов в крови (тромбоцитопения), для устранения этого требуется операция -
удаление селезенки (спленэктомия).
При снижении числа кровяных пластинок, например при
кровопотере, в крови накапливается тромбопоэтин – гликопротеид, стимулирующий
образование пластинок из мегакариоцитов костного мозга.
2.3. Лейкоциты (белые кровяные тельца) – ядерные клетки крови,
выполняющие защитную функцию. Содержатся в крови от нескольких часов до
нескольких суток, а затем покидают кровеносное русло и проявляют свои функции в
основном в тканях.
Лейкоциты в кровяном русле и лимфе способны к активным
движениям, путем образования псевдоподий могут переходить через стенку сосудов
в соединительную ткань органов. Направление движения
лейкоцитов определяется хемотаксисом под влиянием
химических раздражителей – продуктов распада тканей, бактерий и др. Лейкоциты
выполняют защитные функции, обеспечивая фагоцитоз микробов (гранулоциты,
макрофаги), инородных веществ, продуктов распада клеток (моноциты – макрофаги),
участвуя в иммунных реакциях (лимфоциты, макрофаги).
Лейкоцитарная формула – процентное содержание различных форм лейкоцитов (к общему
числу лейкоцитов, равному 100%).
Лейкоциты представляют неоднородную группу, их 5 видов (рис. 19). Зернистые лейкоциты – нейтрофилы, эозинофилы, базофилы.

Рис. 19. Типы лейкоцитов.
Нейтрофилы – самая большая популяция
лейкоцитов (65-75%), их называют микрофагами.
Морфология нейтрофилов:
1) сегментированное ядро;
2) в цитоплазме мелкие
гранулы, окрашивающиеся в слабо оксифильный (розовый) цвет, среди которых можно
выделить неспецифические гранулы – разновидности лизосом, специфические
гранулы Число зерен в каждом нейтрофиле варьирует и составляет
50-200. Имеется аппарат
Гольджи, гранулярный эндоплазматический ретикулум, единичные митохондрии. Размер вмазке
составляет 10-12мкм.
По степени зрелости нейтрофилы подразделяются на:
1) юные (метамиелоциты) – 0-0,5%;
2) палочкоядерные – 3-5%;
3) сегментоядерные (зрелые) – 60-65%.
В нейтрофилах можно различить два типа гранул:
специфические и азурофильные, окруженные одинарной мембраной (рис. 20, А). Специфические
гранулы, более светлые, мелкие и многочисленные, составляют 80-90 % всех
гранул. Их размер около 0,2 мкм, они электронно-прозрачны,
но могут содержать кристаллоид; содержат бактериостатические и бактерицидные
вещества - лизоцим (муромидаза) и щелочную
фосфатазу, а также белок лактоферрин. Лактоферрин
связывает ионы железа, что способствует склеиванию бактерий (бактериальная
мультипликация). Он также инициирует отрицательную обратную связь, обеспечивая
торможение продукции нейтрофилов в костном мозге. Азурофильные гранулы
более крупные (~ 0,4 мкм), окрашиваются в фиолетово-красный цвет; их количество
составляет 10-20 % всей популяции гранул. Они являются первичными лизосомами,
имеют электронно-плотную сердцевину, содержат лизосомальные
ферменты (кислая фосфатаза, β-глюкуронидаза
и др.) и миелопе-роксидазу. Миелопероксидаза из перекиси водорода продуцирует
молекулярный кислород, обладающий бактерицидным действием. Азурофильные гранулы
в процессе дифференцировки нейтрофилов в костном мозге появляются раньше,
поэтому называются первичными в отличие от вторичных
- специфических.
В процессе фагоцитоза бактерий сначала (в течение 0,5-1 мин) с образующейся фагосомой (захваченная бактерия) сливаются специфические гранулы, ферменты которой убивают бактерию, при этом образуется комплекс, состоящий из фагосомы и специфической гранулы. Позднее с этим комплексом сливается лизосома, гидролитические ферменты которой переваривают микроорганизмы. В очаге воспаления убитые бактерии и погибшие нейтрофилы образуют гной.
Продолжительность жизни нейтрофилов – 5 - 9 дней, из
них 8-12 ч они находятся в крови, а затем выходят в соединительную и
эпителиальную ткани, где и выполняют основные функции.
Функции нейтрофилов:
1) фагоцитоз бактерий;
2) фагоцитоз иммунных комплексов («антиген–антитело»);
3) бактериостатическая и бактериолитическая;
4) выделение кейлонов и регуляция размножения лейкоцитов.
Фагоцитарный индекс (число частиц, поглощенных одной клеткой) для
нейтрофилов равен 12-23.
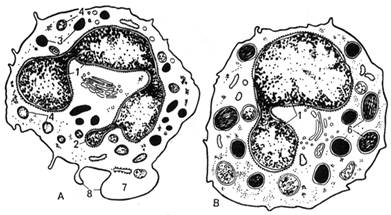
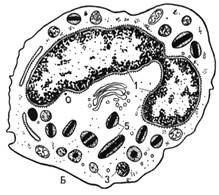
Рис. 20. Ультрамикроскопическое
строение гранулоцитов (схема по Н.А.Юриной и Л.С.Румянцевой). А - сегментоядерный нейтрофил; Б - эозинофил (ацидофильный); В –
базофил (1 - сегменты ядра).
Эозинофилы – 1-5%, размеры в мазках –12-14
мкм.
Морфология эозинофилов:
1) ядро из 2-х сегментов;
2) в цитоплазме отмечается крупная оксифильная (красная) зернистость;
3) другие органеллы развиты слабо (аппарат Гольджи, немногочисленные митохондрии,
актиновые филаменты).
4) среди гранул эозинофилов выделяют
неспецифические азурофильные гранулы – разновидность лизосом, содержащую фермент пероксидазу и
специфические или эозинофильные гранулы, содержащие кислую фосфатазу. Кристаллоиды
эозинофильных гранул содержат главный основной белок (major basic
protein), который участвует в антипаразитарной функции эозинофилов.
По степени зрелости эозинофилы также
подразделяются на юные, палочкоядерные и сегментоядерные, однако определение
этих субпопуляций в клинических лабораториях производится редко.
К
способам нейтрализации гистамина и серотонина относятся фагоцитоз и адсорбция
этих биологически активных веществ на цитолемме, выделение ферментов,
расщепляющих их внеклеточно, выделение факторов, препятствующих выбросу
гистамина и серотонина.
Эозинофилы являются подвижными клетками и способны к
фагоцитозу, однако их фагоцитарная активность ниже, чем у нейтрофилов.
Функция
эозинофилов:
1) участие в иммунологических (аллергических и анафилактических)
реакциях: угнетают (ингибируют) аллергические реакции посредством нейтрализации
гистамина и серотонина;
2) защита от паразитов.
Эозинофилы обладают положительным хемотаксисом к гистамину,
выделяемому тучными клетками (особенно при воспалении и аллергических
реакциях), к лимфокинам,
выделяемым стимулированными Т-лимфоцитами, и иммунным комплексам, состоящим из
антигенов и антител.
Участием эозинофилов в аллергических реакциях объясняется их
повышенное содержание (до 20-40% и более) в крови при различных
аллергических заболеваниях (глистных инвазиях, бронхиальной астме, при раке и
др.).
Эозинофилы способствуют снижению содержания гистамина
в тканях различными путями. Они разрушают гистамин с помощью фермента
гистаминазы, фагоцитируют гистаминсодержащие фанулы тучных клеток, адсорбируют
гистамин на плазмолемме, связывая его с помощью рецепторов, и, наконец,
вырабатывают фактор, тормозящий дегрануляцию и освобождение гистамина из тучных
клеток. Специфической функцией эозинофилов является антипаразитарная. При
паразитарных заболеваниях (гельминтозы, шистосомоз и др.) наблюдается резкое
увеличение числа эозинофилов – до 90 % от общего числа лейкоцитов. Эозинофилы
убивают личинок паразитов, поступившие в кровь или органы (например, в
слизистую оболочку кишки). Они привлекаются в очаги
воспаления хемотаксическими факторами и прилипают к паразитам благодаря наличию
на них обволакивающих компонентов комплемента. При этом происходят дегрануляция
эозинофилов и выделение главного основного белка, оказывающего антипаразитарное
действие. Таким образом, эозинофилы являются первой линией защиты против
паразитов.
Продолжительность жизни
эозинофилов – 6-8
дней, из них нахождение в кровеносном русле составляет 3-8 ч (не более 12 ч). Их
мишенями являются такие органы, как кожа, легкие и гастроинтестинальный тракт.
Базофилы – 0-1%, размеры в мазке – 11-12
мкм. Они так же, как и нейтрофилы, находятся в крови около 1-2 сут.
Морфология базофилов:
1) крупное слабо сегментированное ядро содержит 2-3 дольки;
2) в цитоплазме содержатся очень крупные специфичные гранулы, которые
содержат протеогликаны, гепарин, гистамин,
нейтральные протеазы и другие энзимы;
часть гранул представляет собой модифицированные лизосомы.
3) органеллы развиты слабо (есть эндоплазматическая сеть, рибосомы, аппарат Гольджи,
митохондрии, актиновые филаменты).
Функции
базофилов:
1) участие в иммунных и аллергических реакциях посредством
выделения гранул (дегрануляции) и содержащихся в них вышеперечисленных
биологически активных веществ, которые и вызывают аллергические проявления
(отекткани, кровенаполнение, зуд, спазм гладкой мышечной ткани и др.);
2) фагоцитоз;
3) выделяя
гепарин и гистамин;
4) участвуют в регуляции процессов свертывания крови и
проницаемости сосудов.
Незернистые
лейкоциты – агранулоциты
не содержат в цитоплазме гранул, их
ядра не сегментированы. Делятся на две совершенно
различные клеточные популяции – лимфоциты и
моноциты.
Лимфоциты (20-35% от общего числа лейкоцитов) при участии вспомогательных клеток (макрофагов)
обеспечивают иммунитет, т. е. защиту организма от генетически чужеродных
веществ. Лимфоциты являются единственными клетками крови, способными при
определенных условиях митотически делиться. Все остальные лейкоциты являются
конечными дифференцированными клетками.
По
размерам делятся на:
1) малые (4,5-6
мкм);
2) средние (7-10 мкм);
3) большие (больше 10 мкм).
В
периферической крови до 90% составляют малые лимфоциты и 10-12% – средние. Большие лимфоциты
в периферической крови в норме не встречаются. При электронно микроскопическом
исследовании малые лимфоциты можно подразделить на светлые и темные.
Морфология
лимфоцитов:
1) крупное круглое ядро;
2) в цитоплазме – рибосомы,
эндоплазматическая сеть, комплекс Гольджи,
митохондрии и лизосомы (рис. 21).
По продолжительности жизни лимфоциты подразделяются на:
1) короткоживущие (недели, месяцы) – В
лимфоциты;
2) долгоживущие (месяцы, годы) – Т лимфоциты.
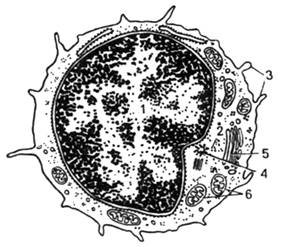
Рис. 21.
Ультрамикроскопическое строение лимфоцита (схема по Н.А.Юриной,
Л.С.Румянцевой). 1 - ядро; 2 - рибосомы;
3 - микроворсинки; 4 - центриоль; 5 - аппарат Гольджи; 6 - митохондрии.
Лимфоциты – гетерогенная (неоднородная) популяция
клеток.
Три основных
функциональных класса:
1) В-лимфоциты
– около 30 % циркулирующих лимфоцитов,
2) Т-лимфоциты
– около 70 % циркулирующих лимфоцитов,
3) нулевые лимфоциты – резервная популяция
недифференцированных лимфоцитов.
В-лимфоциты
впервые были обнаружены в фабрициевой сумке птиц (bursa Fabricius), поэтому и
получили такое название. Они образуются у эмбриона человека из стволовых клеток
- в печени и костном мозге, а у взрослого – в костном мозге. При действии
антигенов В-лимфоциты способны к пролиферации и дифференцировке в плазмоциты
– клетки, способные синтезировать защитные белки - иммуноглобулины
(Ig).
Т-лимфоциты,
или тимусзависимые лимфоциты, образуются из стволовых клеток костного
мозга, а созревают в тимусе (вилочковая железа), что и обусловило их название.
Т-клетки имеют специфические рецепторы, способные распознавать и связывать
антигены, участвовать в иммунных реакциях. Среди Т-лимфоцитов выявлено
несколько функциональных групп: Т-хелперы (начинают иммунный ответ),
Т-супрессоры (завершают иммуннный ответ), Т-киллеры.
Основными функциями Т-лимфоцитов являются обеспечение
реакций клеточного иммунитета и регуляция гуморального иммунитета (стимуляция или
подавление дифференцировки В-лимфоцитов). Т-лимфоциты способны к выработке
лимфокинов, которые регулируют деятельность В-лимфоцитов и других клеток в
иммунных реакциях.
Для Т-лимфоцитов характерно явление рециркуляции, т.е.
выход из крови в ткани и возвращение по лимфатическим путям снова в кровь.
Таким образом, они осуществляют иммунологический надзор за состоянием всех
органов, быстро реагируя на внедрение чужеродных агентов.
Среди клеток, имеющих морфологию малых лимфоцитов,
следует назвать циркулирующие стволовые клетки крови (СКК), которые поступают в
кровь из костного мозга. Впервые эти клетки были описаны А.А.Максимовым и
обозначены им как "подвижный мезенхимный резерв". Из СКК, поступающих в кроветворные органы, дифференцируются
различные клетки крови, а из СКК, поступающих в соединительную ткань
развиваются тучные клетки, фибробласты и др.
Кроме типичных лимфоцитов, в крови человека в
небольшом количестве могут встречаться лимфоплазмоциты (около 1-2 %),
которые отличаются концентрическим расположением вокруг ядра канальцев
гранулярной эндоплазматической сети.
Функции лимфоцитов:
1) В-лимфоциты и образующиеся из них плазмоциты синтезируют антитела,
иммуноглобулины и поэтому обеспечивают гуморальный иммунитет организма от
чужеродных антигенов (бактерий, вирусов, токсинов, белков и др.), содержащихся
в крови, лимфе и тканевой жидкости;
2) Т-лимфоциты отвечают за клеточный иммунитет и регулируют
гуморальный.
Однако эта простая классификация устарела, и сейчас принято все
лимфоциты классифицировать по наличию на их мембране рецепторов (CD). В
соответствии с этим выделяют лимфоциты CD3, CD4, CD8 и т. д.
Моноциты (6-8 % от общего числа лейкоцитов) – самые крупные клетки крови (18-20 мкм), они имеют крупное бобовидное
или подковообразное ядро и хорошо выраженную базофильную цитоплазму, в ней
множественные пиноцитозные пузырьки, лизосомы и другие общие органеллы (ЭПС,
АГ, митохондрии) (рис. 22).
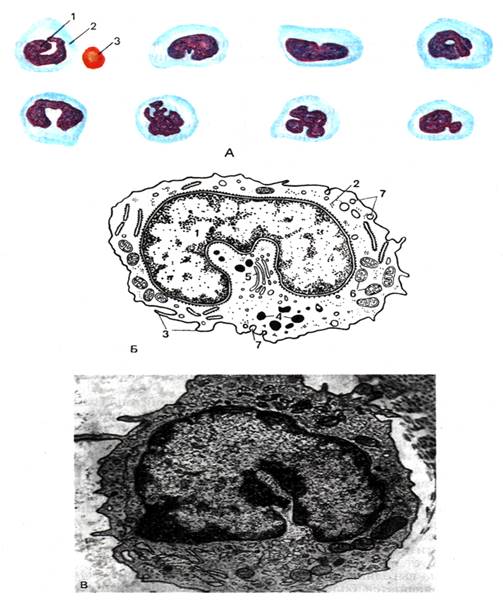
Рис. 22. Строение
моноцитов.
А
- разновидности моноцитов по размерам и форме в мазке крови человека. Окраска
по Романовскому-Гимзе (по Ю.И.Афанасьеву); Б - схема ультрамикроскопического
строения моноцитов (по Н.А.Юриной, Л.С.Румянцевой); В - электронная
микрофотография, × 15 000 (по НА.Юриной,
А.И.Радостиной): 1 - ядро; 2 - рибосомы; 3 - микроворсинки; 4 - лизосомы; 5 -
аппарат Гольджи; 6 - митохондрии; 7 - пиноцитозные пузырьки.
Функция моноцита: фагоцитоз. Моноциты относятся к
макрофагической системе организма, или к так называемой мононуклеарной
фагоцитарной системе (МФС). Клетки этой системы характеризуются
происхождением из промоноцитов костного мозга,
активностью пиноцитоза и иммунного фагоцитоза, наличием на мембране
рецепторов для иммуноглобулинов и комплемента. Моноциты циркулирующей крови
представляют собой подвижный пул относительно незрелых клеток, находящихся на
пути из костного мозга в ткани. Время пребывания моноцитов в крови варьирует от
36 до 104 ч (обычно 2-3 сут), после чего покидают
кровеносное русло, мигрируют в разные ткани и органы и превращаются в различные
формы макрофагов, фагоцитарная активность которых значительно выше моноцитов.
Моноциты и образующиеся из них макрофаги объединяются в единую макрофагическую
систему (или мононуклеарную фагоцитарную систему (МФС)).
Моноциты, выселяющиеся в ткани, превращаются в макрофаги,
при этом у них появляются большое количество лизосом, фагосом, фаголизосом.
3. Особенности
формулы крови у детей
У новорожденных в общем анализе крови эритроцитов 6–7×1012 /л – физиологический эритроцитоз, количество
гемоглобина достигает 200 г/л, лейкоцитов 10–30×109/л – физиологический возрастной лейкоцитоз,
количество тромбоцитов такое же, как и у взрослых – 200–300×109/л.
После
рождения количество эритроцитов и гемоглобина постепенно снижается, достигая сначала
показателей взрослых (5 млн в 1 мкл), а затем
развивается физиологическая анемия. Уровень эритроцитов и гемоглобина достигает
показателей взрослых только к периоду полового созревания. Количество
лейкоцитов через 2 недели после рождения снижается до 10–15×109/л, а к периоду полового
созревания достигает значений взрослого человека.
Наибольшие изменения в лейкоцитарной формуле у детей отмечаются в
содержании лимфоцитов и нейтрофилов. Остальные показатели не отличаются от
значений взрослых.
При
рождении соотношение нейтрофилов и лимфоцитов аналогично показателям взрослых
– 65-75% к 20-35%. В первые дни жизни ребенка наблюдается снижение
концентрации нейтрофилов и повышение содержания лимфоцитов, на 4-5-е сутки их
количество сравнивается – по 45% (первый физиологический перекрест). Далее у
детей наблюдаются физиологический лимфоцитоз – до 65% и физиологическая
нейтропения – 25%, наиболее низкие показатели нейтрофилов наблюдаются к концу
второго года жизни. После этого начинается постепенное повышение содержания
нейтрофилов и снижение концентрации лимфоцитов, в возрасте 4–5 лет
наблюдается второй физиологический перекрест. К периоду полового созревания
соотношение нейтрофилов и лимфоцитов приходит к уровню взрослого человека.
Число лейкоцитов у новорожденных увеличено и достигает
10,0–30,0×109/л.
В течение 2 нед после рождения число их падает до 9,0–15,0×109/л, а к к 14–15 годам достигает уровня, который сохраняется у
взрослого.
Соотношение числа нейтрофилов и лимфоцитов у новорожденных
такое же, как и у взрослых 4,5–9,0×109/л. В последующие сроки
содержание лимфоцитов возрастает, а нейтрофилов падает, и, таким образом, к 4-м
суткам количество этих видов лейкоцитов уравнивается (первый
физиологический перекрест лейкоцитов). Дальнейший рост числа лимфоцитов
и падение нейтрофилов приводят к тому, что на 1–2-м
году жизни лимфоциты составляют 65%, а нейтрофилы –
25%. Новое снижение числа лимфоцитов и повышение нейтрофилов приводят к
выравниванию обоих показателей у 4-летних
детей (второй физиологический перекрест). Постепенное
снижение содержания лимфоцитов и повышение нейтрофилов продолжаются до полового
созревания, когда их количество достигает нормы взрослого.
4.
Кроветворение (гемопоэз)
Кроветворение (гемопоэз) – процесс образования
форменных элементов крови. Развитие эритроцитов называют эритропоэзом,
развитие гранулоцитов – гранулоцитопоэзом, тромбоцитов – тромбоцитопоэзом,
развитие моноцитов – моноцитопоэзом, развитие лимфоцитов и иммуноцитов
– лимфоцито- и иммуноцитопоэзом.
Различают два ряда
кроветворения:
1) миелоидное; 2) лимфоидное.
В свою очередь миелоидное
кроветворение подразделяется на:
1) эритроцитопоэз; 2) гранулоцитопоэз; 3) тромбоцитопоэз; 4) моноцитопоэз.
Кроме того, гемопоэз подразделяется на два
периода:
1) эмбриональный; 2) постэмбриональный.
Эмбриональный гемопоэз приводит к
развитию крови как ткани, а постэмбриональный гемопоэз представляет собой
процесс физиологической регенерации крови.

Рис. 23.
Эмбриональный гемопоэз.
В развитии крови как ткани в эмбриональный период
можно выделить 3 основных этапа, последовательно
сменяющих друг друга:
1) мезобластический – развитие
клеток крови во внезародышевой мезенхиме стенки желточного мешка, хориона и стебля
(с 3-й по 9-ю неделю развития зародыша человека) и появляется первая генерация
стволовых клеток крови (СКК), эритроциты и гранулоциты;
2) гепатоспленотимический – в печени
(с 5-6-й недели развития плода, достигает максимума через 5 мес
и завершается перед рождением) – эритроциты, гранулоциты, мегакариоциты, селезенке (начиная с 7-8-й недели, развиваются – эритроциты,
гранулоциты, лифоциты), тимусе (с 12-й недели – Т
лимфоциты) и лимфатические узлы (гемопоэз отмечается с 10-й недели -
лимфоциты);
3) медуллярный (костномозговой) – с 10-12-й недели и постепенно
нарастает к рождению, а после рождения костный мозг становится центральным
органом гемопоэза и остается им в течение постнатальной жизни. Он обеспечивает
стволовыми кроветворными клетками тимус и другие гемопоэтические органы.
Постэмбриональный
гемопоэз представляет собой процесс физиологической регенерации
крови (клеточное обновление), который компенсирует физиологическое
разрушение дифференцированных клеток. Осуществляется
в красном костном мозге и лимфоидных органах (тимусе, селезенке, лимфоузлах,
миндалинах, лимфоидных фолликулах).
Миелопоэз
происходит в миелоидной ткани, расположенной в эпифизах трубчатых и полостях
многих губчатых костей. Здесь развиваются форменные элементы крови: эритроциты,
гранулоциты, моноциты, кровяные пластинки, предшественники лимфоцитов. В
миелоидной ткани находятся стволовые клетки крови и соединительной ткани.
Предшественники лимфоцитов постепенно мигрируют и заселяют такие органы, как
тимус, селезенка, лимфатические узлы и др.
Лимфопоэз
происходит в лимфоидной ткани, которая имеет несколько разновидностей,
представленных в тимусе, селезенке, лимфатических узлах. Она выполняет основные
функции: образование Т- и В-лимфоцитов и иммуноцитов
(плазмоцитов и др.).
Совокупность
клеток, составляющих линию дифференцировки стволовой клетки в определенный
форменный элемент, образует дифферон (или гистогенетический ряд). Например,
эритроцитарный дифферон составляют:
1) стволовая клетка (I класс);
2) полустволовая клетка – предшественница миелопоэза (II класс);
3) унипотентная эритропоэтинчувствительная клетка (III класс);
4) эритробласт (IV класс);
5) созревающая клетка – пронормоцит, базофильный нормо цит, полихроматофильный
нормоцит, оксифильный нормоцит, ретикулоцит (V класс);
6) эритроцит (VI класс).
5. Лимфа
Лимфа (лат. lympha
– влага) представляет собой слегка желтоватую жидкость белковой природы,
протекающую в лимфатических капиллярах и сосудах.
Образуется лимфа из тканевой жидкости, поступившей в
лимфатические капилляры и сосуды. Из капилляров лимфа перемещается в
периферические лимфатические сосуды, по ним - в лимфатические узлы, затем в
крупные лимфатические сосуды и вливается в кровь (рис. 24).
В сутки образуется 2-4 л лимфы в организме взрослого
человека.
Лимфа состоит из лимфоплазмы (plasma lymphae) и форменных элементов.
Форменные
элементы лимфы:
1) лимфоциты – 98 %,
2) моноцитами и другими видами лейкоцитов – 2%,
3) эритроцитов нет, иногда – единичные.
Плазма лимфы по химическому составу близка к плазме крови, но отличается:
1) в 3-4 раза меньше белков, альбумины преобладают над
глобулинами, часть белка составляют ферменты – диастаза, липаза и
гликолитические ферменты, есть фибриноген и может сворачиваться;
2) липидов в ней больше, так как они всасывается из
тонкого кишечника после переваривания в лимфу, а не в кровь;
3) щелочная среда.
Функции лимфы и лимфатической системы:
1) дренажная: дренирование тканей
(отток жидкости от тканей);
2) кроветворная: созревание лимфоцитов и обогащение лимфы
лимфоцитами из лимфоузлов;
3) защитная
или иммунная: обеззараживание лимфы, удаление из
нее от вредных веществ и микробов
лимфоцитами;
4) метаболическая: участие в водно-солевом и липидном обмене,
транспорте веществ.
5) Гомеостатическая: все эти функции обеспечивают гомеостаз или постоянство внутренней среды организма.

Рис. 24. Лимфатическая система.