Транспорт газов кровью
Переносчиком
кислорода от легких к тканям и углекислого газа от тканей к легким является
кровь. Кислород переносится с кровью в растворенном виде (небольшое количество)
и в соединении с гемоглобином (основное количество кислорода).
Транспорт кислорода. Кислород,
растворяющийся в плазме крови капилляров малого круга кровообращения,
диффундирует в эритроциты, сразу связывается с гемоглобином, образуя
оксигемоглобин. Скорость связывания кислорода велика: время полунасыщения гемоглобина
кислородом около 3 мс. Один грамм гемоглобина связывает 1,34 мл кислорода, в
100 мл крови 16 г гемоглобина и, следовательно, 19,0 мл кислорода. Эта
величина называется кислородной емкостью крови (КЕК).
Превращение
гемоглобина в оксигемоглобин определяется напряжением растворенного кислорода.
Графически эта зависимость выражается кривой диссоциации оксигемоглобина, или
сатурационной кривой (сатурация – насыщение жидкости газами) (рис. 28).
На рисунке
видно, что даже при небольшом парциальном давлении кислорода (40 мм рт. ст.) с
ним связывается 75-80% гемоглобина.
Кривая диссоциации имеет S-образную форму и состоит из двух
частей – крутой и отлогой. Отлогая часть кривой, соответствующая высоким (более
60 мм рт. ст.) напряжениям кислорода, свидетельствует о том, что в этих
условиях содержание оксигемоглобина лишь слабо зависит от напряжения кислорода
и его парциального давления во вдыхаемом и альвеолярном воздухе. Верхняя отлогая
часть кривой диссоциации отражает способность гемоглобина связывать большие
количества кислорода, несмотря на умеренное снижение его парциального
давления.
При давлении 80-90 мм рт. ст.
гемоглобин почти полностью насыщается кислородом парциального давления во
вдыхаемом воздухе. В этих условиях ткани достаточно снабжаются кислородом
(точка насыщения).
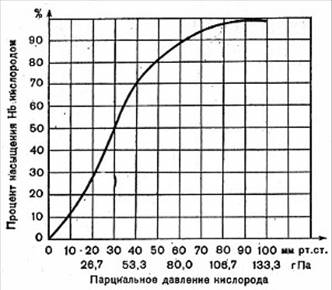
Рис. 29. Кривая
диссоциации оксигемоглобина
Крутая часть
кривой диссоциации соответствует напряжению кислорода, обычному для тканей
организма (35 мм рт. ст. и ниже). В тканях, поглощающих много кислорода
(работающие мышцы, печень, почки), оксигемоглобин диссоциирует в большей
степени, иногда почти полностью. В тканях, в которых интенсивность окислительных
процессов мала, большая часть оксигемоглобина не диссоциирует.
Свойство
гемоглобина – легко насыщаться кислородом даже при небольших давлениях и легко
его отдавать – очень важно. Благодаря легкой отдаче гемоглобином кислорода при
снижении его парциального давления обеспечивается бесперебойное снабжение
тканей кислородом, в которых вследствие постоянного потребления кислорода его
парциальное давление равно нулю.
Распад
оксигемоглобина на гемоглобин и кислород зависит от:
1)
температуры (увеличивается с
повышением температуры тела).
2)
реакции среды плазмы крови (с
увеличением кислотности среды увеличивается диссоциация оксигемоглобина)
3)
содержания солей (в воде связывание
гемоглобина осуществляется быстро, но полного насыщения не достигается, более
полное насыщение кислородом и более полная отдача кислорода происходит в
физиологическом растворе).
4)
содержания в крови продуктов распада
(способствуют более быстрой диссоциации).
5)
содержания углекислого газа (чем
больше содержание СО2 в крови, тем меньше связывается гемоглобин с О2
и тем быстрее происходит диссоциация оксигемоглобина).
Кривая диссоциации оксигемоглобина смещается вправо при увеличении
температуры, снижении рН и повышении содержания 2,3 – ДФГ (капилляры большого
круга кровообращения). Т.е в этих условиях сродство гемоглобина к кислороду
снижается. При увеличении рН, снижении температуры тела и 2,3-ДФГ происходит сдвиг
кривой влево (капилляры малого круга кровообращения) (рис. 30).
Особенно
резко понижается способность гемоглобина соединяться с кислородом при давлении
углекислого газа, равном 46 мм рт. ст., т.е. при величине, соответствующей
напряжению углекислого газа в венозной крови. Влияние углекислого газа на
диссоциацию оксигемоглобина очень важно для переноса газов в легких и тканях.
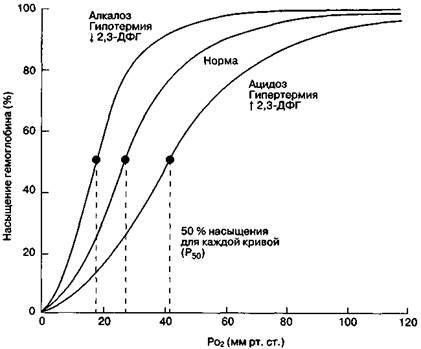
Рис. 30. Сдвиги кривой
диссоциации оксигемоглобина при изменениях рН, температуры тела и концентрации
2,3-дифосфоглицерата (2,3-ДФГ) в эритроцитах
 При подготовке к серьезным соревнованиям во время
разминки, даже в теплое время года спортсмены одевают утепленные костюмы
(разогревают мышцы). Зачем необходимо разогревать мышцы?
При подготовке к серьезным соревнованиям во время
разминки, даже в теплое время года спортсмены одевают утепленные костюмы
(разогревают мышцы). Зачем необходимо разогревать мышцы?
Транспорт
углекислого газа. Двуокись углерода переносится кровью
двумя основными способами:
1) физическим (растворением)
2) химическим.
Растворённый в плазме крови СО2
составляет около 5% общего количества транспортируемого кровью углекислого
газа. 95% СО2 переносится в форме химической связи с другими
веществами, содержащимися в крови.
Углекислый газ
находится в крови в одной из трёх химических форм:
1)угольная кислота (Н2СО3),
2) бикарбонатный ион
(НСО3-)
3) карбгемоглобин (HbCO2).
Связывание
СО2 кровью в капиллярах большого круга. Помимо
небольшого количества СО2, который попадая в кровь, физически
растворяется в её плазме, почти весь остальной углекислый газ, проникающий в
плазму капиллярной крови из тканевой жидкости сразу же диффундирует в
эритроциты, где осуществляются две основные химические реакции, связывающие СО2.
1-я
реакция - реакция
гидратации СО2 - связывание СО2 с водой с
образованием угольной кислоты (Н2СО3):
СО2 +
Н2О ⇄ Н2СО3
Эта реакция
катализируется ферментом – карбоангидразой;
участие фермента ускоряет реакцию в 250 раз. Как только образуется угольная
кислота, она немедленно ионизирует, т.е. диссоциирует на водородный ион (Н+)
и бикарбонатный ион (![]() ):
):
Н2СО3
⇄
Н+ + ![]()
Следовательно,
содержание угольной кислоты в крови ничтожно мало. Полностью 1-я реакция может
быть записана следующим образом:
СО2 + Н2О ⇄
Н2СО3 ⇄ Н+ +
![]()
Таким образом, в
результате 1-й реакции гидратации образуются бикарбонатные ионы, в составе
которых переносится более 4/5 всего содержащегося в венозной крови СО2.
По мере повышения концентрации бикарбонатных ионов в эритроците они
диффундируют в плазму, где соединяются с ионами Na+,
образуя бикарбонат натрия (NaНСО3).
Последний действует как буферный агент, предотвращающий повышение кислотности
(снижение рН) крови, особенно в связи с поступлением в кровь молочной кислоты (HLa) при мышечной работе.
HLa
+ NaНСО3
⇄NaLa + Н2СО3 ⇄
Н2О + СО2↑
2-я реакция:
связывание СО2 с белками крови и образование карбаминовых
соединений. Небольшая часть СО2 связывается прямо в плазме с её
белками. Однако в основном эта реакция осуществляется внутри эритроцитов, где
СО2 соединяется с гемоглобином, образуя карбгемоглобин. СО2
реагирует с глобином, не затрагивая частиц гема, которые сохраняют возможность
связи с О2.
Отдача
СО2 кровью в
лёгочных капиллярах. В крови альвеолярных капилляров наблюдается серия
противоположных по направлению реакций, которые происходят в основном в
эритроцитах и приводят к освобождению СО2 из химических связей и
выходу его из крови. Главная из них – реакция
дегидратации – совершается в эритроцитах с участием карбоангидразы:
Н+ + ![]() ⇄ Н2СО3
⇄
Н2О + СО2
⇄ Н2СО3
⇄
Н2О + СО2
Благодаря непрерывному
устранению конечного продукта (выходу СО2 из эритроцитов) реакция
идёт слева направо, как и другая реакция – диссоциация карбгемоглобина с
освобождением СО2 и присоединением О2 к восстановленному
гемоглобину:
О2 + H HbCO2⇄
H
HbO2
+ CO2
⇄
HbO2
+ Н+ + СО2
|
|
|
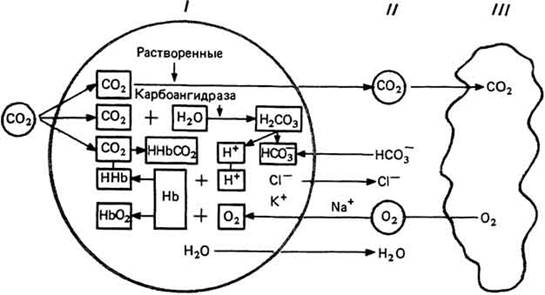
Рис. 31. Реакции, происходящие в процессе обмена кислородом и
углекислым газом между эритроцитом (I), плазмой (II) и
легочной альвеолой (III).