ЛЕКЦИЯ № 5
ВЕЩЕСТВЕННЫЙ СОСТАВ ЗЕМЛИ
Химический состав земной коры.
На Земле
установлено около 300 химических элементов и их изотопов. Изотопы (греч. «исос» - равный,
«топос» - место) обладают теми же свойствами, зарядом ядра и
порядковым номером, что и
соответствующий химический элемент, но отличаются от него атомным весом.
Земную
кору слагают различные материальные тела, состоящие из определенного сочетания химических элементов и их соединений. Такие соединения образуют
естественные природные тела - минералы, которые входят в состав горных пород. Минералы и горные породы в различных сочетаниях образуют слои, фации, формации и т.п., а их
совокупность составляет
земную кору. Этим самым определяются нижняя и
верхняя ступени различимости объекта геологии
(минерал -
земная кора). Состав земной коры изучают
методами физико-химического
анализа образцов горных пород и минералов,
доставленных из естественных обнажений и
горных выработок (шахты,
скважины и т.п.), а также поднятых со дна океана.
|
|
Для
изучения среднего химического состава Земли используются образцы, доставленные с Луны, а также
метеориты. Следовательно,
прежде чем перейти к систематическому обзору минералов и горных пород, необходимо познакомиться с некоторыми
сведениями о химическом составе Земли и основных геосфер.
Химический состав земной коры.
Вычисления
среднего химического состава внутренних оболочек Земли, в том числе и земной коры, выполнялись многими
исследователями. В зависимости от принятой гипотезы эволюции Земли, используемых методов, а также, учитывая масштабы объекта и недоступность
глубоких слоев для непосредственного анализа, результаты оценок химического
состава геосфер расходятся в определенном диапазоне значений.
Наиболее часто цитируемые
значения химического состава внешних и
внутренних сфер Земли приведены в таблице 2.
Таблица 2.
Средний химический состав геосфер (в
массовых %).
|
Элемент |
Земная коря |
Гидросфера |
Атмосфера |
Биосфера (живое вещество) |
|
Кислород |
49,13 |
85,70 |
20,95 |
70,00 |
|
Кремний |
26,00 |
- |
- |
|
|
Алюминий |
7,45 |
- |
|
_ |
|
Железо |
4.2(1 |
- |
- |
- |
|
Кальций |
3,25 |
- |
- |
0,50 |
|
Натрий |
2,40 |
1,05 |
- |
- |
|
Калий |
2.35 |
- |
|
3,30 |
|
Магний |
2,35 |
0,13 |
- |
|
|
Водород |
1,00 |
10,80 |
- |
10,50 |
|
Титан |
0,61 |
- |
- |
- |
|
Углерод |
0,35 |
- |
|
18,00 |
|
Хлор |
- |
1,90 |
- |
18,00 |
|
Азот |
- |
|
78,08 |
0,31 |
|
Аргон |
i |
- |
0,93 |
- |
В
основе приведенной таблицы - перечень преобладающих в земной коре химических
элементов (с точностью до десятых процента, при меньших количествах - прочерк).
Суммарное содержание элементов в каждой колонке (геосфере) превышает 99%. Однако при переходе из одной геосферы в другой (от земной коры к биосфере) количественный
и качественный состав преобладающих элементов
существенно трансформируется; в земной
коре преобладает 11 элементов, в
гидросфере - 5, в атмосфере - 3, а в биосфере число элементов вновь возрастает до 7.
Несмотря
на образование всех геосфер из одного источника - вещество мантии, состав и соотношение элементов в них корректируется фазовым состоянием
(твердое, жидкое, газообразное) и положением геосферы r круговороте
вещества в географической оболочке.
В
Исследователи приводят
разные данные о химическом составе земной коры. Существенно преобладают три элемента: кислород (46,6-49,1%), кремний (26,0-29,5%), алюминий
(7,45-8,14); на долю еще шести элементов приходится 15 %: железо (4,20-5,00),
кальций (2,71-3,63), натрий (2,01-2,83), калий (2,35-2,59), магний
(1,79-2,35%)и титан. На долю остальных элементов приходится менее
1%. В природе встречаются участки, в
пределах которых фактическое содержание того или иного химического элемента существенно выше его кларкового значения. Такие участки исследуются геологами с целью
выявления месторождении полезных ископаемых.
Химический
состав Земли не постоянен. С одной стороны, земная кора непрерывно пополняется космическим веществом. Оно выпадает на Землю в виде метеоритов и космической пыли. С другой
стороны, сама Земля отдает в мировое пространство часть своего вещества,
например гелий, неон, возможно, водород, азот и другие газообразные элементы и
соединения.
Кроме того, некоторые
химические элементы, например, радиоактивные, со временем изменяются. Так,
уран и торий, распадаясь, превращаются в
устойчивые элементы — свинец и гелий. Это дает основание предполагать,
что в минувшие геологические эпохи кларки урана и тория были, очевидно,
значительно выше, а кларки свинца - ниже, чем сейчас. По-видимому, это
относится и ко всем другим элементам, подверженным превращениям.
Изотопный состав некоторых
химических элементов со временем меняется. Изотоп урана U238 имеет период полураспада (в годах), равный 4,5x109, a U235 - 7,1x108 степени. По А.А. Саукову, два млрд. лет назад атомов изотопа U235 на Земле было почти в шесть раз больше, чем сейчас.
Более
сложный и разнообразный состав имеет живое вещество биосферы, поскольку в жизненных процессах синтезируется вещество трех остальных геосфер.
Каркас органического
вещества составляет углерод в самых разнообразных
сочетаниях с
атомами водорода, кислорода, азота, фосфора и других элементов.
Главной особенностью
химического состава земной коры, по
сравнению с ядром и мантией, является высокое содержание в ней относительно
легких элементов (О, Si, A1,
К, Са) и низкое - тяжелых: (Fe, Ni, Cr, Co).
Такое распределение химических
элементов обусловлено главным образом особенностями образования земной коры, как структурной части Земли, и
свойствами самих химических элементов.
Содержащиеся
в земной коре химические элементы во взаимодействии между собой образуют
различные по сложности структурные образования. По линии возрастания сложности иерархия (соподчинение) таких
структурных образований
может быть представлена следующим рядом: химический
элемент -> минерал -> горная порода -> формация -> земная кора.
Химический состав земной
коры непрерывно меняется и этот процесс продолжается и в настоящее время. Эти
изменения протекают за счет как
внутриземных процессов (радиоактивный
распад), так и внешних факторов,
например, поступление
метеоритного вещества.
Составляющие вещество земной
коры химические элементы образуют разнообразные сочетания. Наиболее
распространенной формой существования сочетаний химических элементов является минерал. Часть из этих
элементов образует самостоятельные минералы, другие входят в них в
качестве примесей.
Минералы и их
морфология
Минералом
(от лат. "минера" - руда)
называется природное соединение химических элементов (или самородный элемент),
возникающее в результате определенных физико-химических процессов, протекающих
в земной коре или на ее поверхности.
К
настоящему времени известно около 4000 минералов, из них наиболее широко распространены 400-500
видов. Изучением химического
состава минералов, их физических свойств и происхождения занимается специальный раздел геологии - минералогия.
По
своему внутреннему строению, проявляющемся во внешнем облике, все минералы
делятся на две группы - кристаллические
и аморфные.
Кристалл
(от греч. "кристаллос" - лед,
горный хрусталь) -
твердое природное тело, имеющее естественную форму правильного многогранника
вследствие упорядочение закономерного расположения
атомов, образующих трехмерную периодически повторяющуюся
укладку - кристаллическую решетку
(рис. 7).
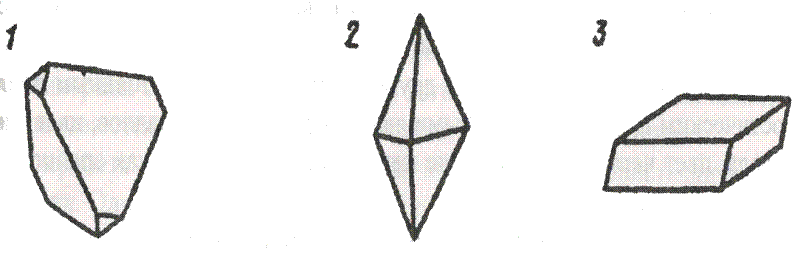
Рис.7. Кристаллические формы минералов: I - равновытянутый кристалл сфалерита (тетраэдр); 2 - вытянутый в одном направлении кристалл серы
(пирамидальный); 3 - вытянутый в двух направлениях кристалл кальцита
(ромбоэдр)
Кристаллы обладают
симметрией внешней формы. Атомы и ионы в кристаллической
решетке располагаются в постоянных точках (узлах) - в строго
определенном для каждого минерала порядке. Углы между гранями кристалла также
всегда постоянны. Основными элементами кристаллической решетки являются центры, оси и плоскости симметрии.
Плоскость
симметрии делит фигуру кристалла на две зеркально-подобные части. При повороте кристалла
вокруг оси симметрии эта фигура совмещается сама с
собой. Минимальный по объему параллелепипед, отражающий
все характерные особенности кристалла, называется «элементарной ячейкой». Основными
кристаллографическими константами такой ячейки являются ребра и углы между
ними. Изучение их взаимоотношений позволило установить 32 класса симметрии кристаллов.
Каждый кристалл ограничен
гранями одной или нескольких простых форм (рис.8, 9). Среди них по степени
симметрии выделяют семь сингоний (греч. «син» - вместе, «гониа» - угол). Высшая сингония – кубическая
(рис. 8, 10). В ней ребра кристаллов расположены под прямыми углами по
трем осям координат и равны между собой. К
низшим сингониям относятся ромбическая,
моноклинная, триклинная. Они характеризуются неравенством ребер, прямыми
(ромбическая) или не равными 90° углами. Средние
- это тетрагональная (ребра по двум осям равны, все углы прямые),
гексагональная (ребра по двум осям равны, два угла прямые, один равен
120°) (рис.10) и тригональная
(все ребра равны, углы не равны
90°) сингонии.
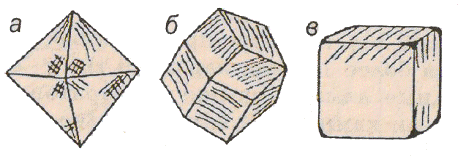
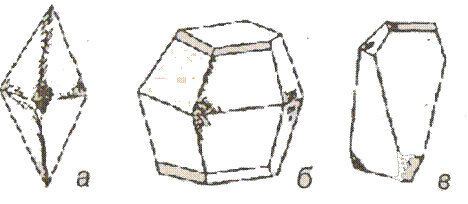
Рис. 8. Формы кристаллов алмаза: Рис.
9. Кристаллические формы серы:
а – октаэдр; б –ромбододекаэдр; а
– пирамидального облика;
в – куб.
б –
усеченно-пирамидального облика;
в – ромбо-тетраэдрического облика
Подсчитано,
что около 38% минералов кристаллизуется в триклинной и моноклинной, 23% - в ромбической, 10% - в
тригональной, 7,5% - в гексагональной,
9,5% - в тетрагональной. 12% - в кубической сингониях.
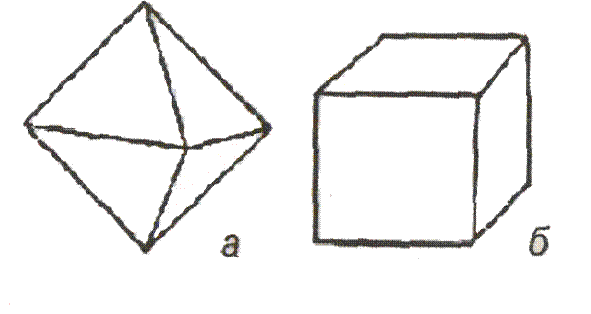
Рис. 10. Кристаллы флюорита: гексагональный (а) и кубический (б).
Аморфными (от греч. "аморфос" - бесформенный) называют минералы, в которых составляющие их частицы
(атомы, молекулы, ионы) располагаются беспорядочно, хаотично, т. е не образуют
кристаллическую решетку.
Для
различения этих двух типов минералов можно использовать
образ строительных кирпичей в качестве химических
элементов: куча кирпичей - аморфное тело; стена, уложенная из этих же кирпичей в определенном порядке - кристаллическое тело.
Минералы
могут быть твердыми, жидкими (ртуть)
и газообразными
(метан, сероводород).
Подавляющее
большинство твердых минералов представлено кристаллическими телами и лишь незначительная их часть - аморфные минералы. Кристаллические
минералы обладают
способностью самоограняться, т.е. давать правильно образованные кристаллические многогранники, а
аморфные дают обычно бесформенные массы и обломки. В природе минералы чаще всего встречаются в
виде кристаллических
скоплений - агрегатов и значительно реже в виде правильных многогранников - кристаллов. В
благоприятных условиях свободного роста кристаллы приобретают свойственную им
форму правильного многогранника, а в условиях взаимостесненного роста образуется агрегат кристаллов.
Поскольку
форма кристаллов не всегда хорошо выражена, приходится обращаться к другим признакам и методам определения
минералов, которые делятся на полевые и лабораторные. При полевых геологических работах главнейшие
минералы определяются по комплексу физических свойств и признаков, зависящих от условий их
образования и химического состава. К основным физическим
свойствам относятся
следующие визуально определяемые признаки: агрегатное состояние, цвет, блеск, цвет черты на
фарфоровой пластине, твердость, спайность,
излом, прозрачность и другие характерные
индивидуальные для минералов свойства. Характеристики полевого определения свойств минералов дополняются лабораторным анализом химического
состава, оптических свойств, рентгеноструктурного анализа и др.
Распределение
минералов в земной коре
закономерно связано с условиями их образования.
Первоисточником минералообразования является магма - высокотемпературный расплав вещества астеносферы,
проникающий в земную кору или изливающийся на поверхность. В зависимости от места остывания магмы и
выделяющихся из них паро-водяных
растворов образуются различные минералы. Важнейшими для образования минералов
характеристиками являются температура
и давление в месте остывания расплава и растворов Известно, что переход воды в
пар возможен при давлении не выше
218 атм. (критическое давление).
Кроме критического давления существует и критическая температура, при которой вода переходит в пар независимо от давления. Для чистой воды эта температура
равна 374˚С, которую еще
называют абсолютной температурой кипения.
В зависимости от концентрации растворов критические значения температуры и давления несколько повышаются. Поскольку температура и давление с глубиной
растут, в земной коре возникает несколько горизонтов образования определенных комплексов минералов (рис. 11)
По
условиям и месту образования (снизу вверх в земной коре) выделяют следующие
генетические (генезис - происхождение) типы минералов магматический,
пегматитовый, пневматолитовый, гидротермальный и гипергенный.
Магматический
тип. Минералы образуются
при остывании магмы в земной коре при температуре около 1000°С. На ранних стадиях остывания выделяются оливин,
пироксены, плагиоклазы, позже
- слюды, ортоклаз и в последнюю
очередь - кварц.
Пегматитовый
тип. Минералы образуются
при остывании последних
порций магмы, внедрившейся в трещины земной коры при температурах 500-700°С.
В эту стадию остывания магмы
образуются кварц, полевой шпат, многие
рудные минералы, драгоценные камни и радиоактивные
элементы.
Пневматолитовый
тип. Минералы образуются
в трещинах и разломах земной коры выше пегматитовых
жил в результате остывания
перегретого пара, содержащего сернистые, фтористые и хлористые соединения различных металлов при температурах от критических 374°С
до 500˚С. В эту стадию
остывания образуются
минералы, содержащие руды
вольфрама, мышьяка, молибдена, висмута и др.
![]()
![]()
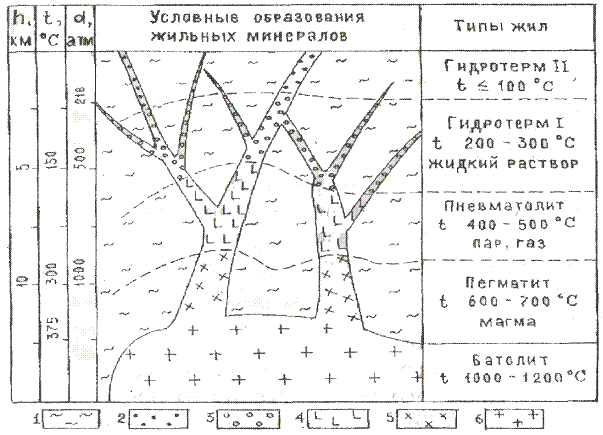
![]() Рис. 11. Схема
жильного минералообразования:
Рис. 11. Схема
жильного минералообразования:
![]() 1 – осадочные и
метаморфические породы коры;
1 – осадочные и
метаморфические породы коры;
![]() 2 – зона
низкотемпературных гидротерм;
2 – зона
низкотемпературных гидротерм;
![]() 3 – зона
высокотемпературных (докритических) гидротерм;
3 – зона
высокотемпературных (докритических) гидротерм;
![]() 4 –
пневматолитовые минералы сверхкритических температур (>374˚С);
4 –
пневматолитовые минералы сверхкритических температур (>374˚С);
![]() 5 – пегматитовые
минералы (расплав магмы);
5 – пегматитовые
минералы (расплав магмы);
![]() 6 – гранитный
батолит.
6 – гранитный
батолит.
Гидротермальный
тип. При температурах
ниже критических (<374°С) и давлениях выше
критических (более 218 атм.) водяной пар
конденсируется в горячие водные растворы,
циркулирующие вдоль трещин в земной коре выше горизонта пневматолиза. При остывании растворов и их взаимодействии с вмещающими породами образуются весьма распространенные и характерные гидротермальные жилы, содержащие ценные руды металлов (золото, серебро,
ртуть, свинец, цинк и др.): галенит,
сфалерит, киноварь, пирит и др.
Гипергенный
тип. Минералы этого типа
образуются в самых верхних слоях
земной коры при температурах ниже кипения, а также в морях, озерах и болотах в
результате химических реакций и роста концентрации растворов (охлаждение, испарение и др.). Для этого типа
характерны минералы карбонатов (кальцит, доломит), сульфатов (мирабилит), галоидов
(галит, сильвин) и др.
Переход
из одного "этажа" минералообразования на другой (от магматического до гипергенного) происходит постепенно, поэтому возможны и смешанные комплексы минералов, Более того, многие минералы (кварц,
кальцит, пирит и др.) образуются в широком
диапазоне температур и давлений и такие
минералы часто называют сквозными. Например, кварц образуется во всех диапазонах температур и давлений. Только сочетание минерального комплекса позволяет
определить место и условия их образования. Совместное образование минералов в одних и тех же условиях принято
называть парагенезисом, что нередко позволяет прогнозировать и вести поиск одних минералов по другим.
Внутреннее
строение и химический состав минералов определяют их физические свойства. Это - плотность, теплопроводность,
электропроводность, радиоактивность, а также механические, оптические, люминесцентные, магнитные и др. свойства.
Минералы
отличают друг от друга по иx внешним постоянным диагностическим признакам. Таковыми являются: облик
кристаллов, цвет минерала,
цвет черты, а также такие механические свойства, как спайность, твердость и др.
Облик
кристаллов - это их форма. Различают кристаллы, вытянутые в одном направлении
(призматические, столбчатые, игольчатые, волокнистые); вытянутые в двух
направлениях (таблитчатые, пластинчатые, листоватые, чешуйчатые) и одинаково развитые по трем
измерениям - изометричные
(куб, октаэдр и др.).
Цвет - обычно постоянный
признак минерала. Но иногда один и тот же
минерал бывает окрашен в различные цвета. Например, кварц бесцветен (горный хрусталь). Но некоторые разновидности
его окрашены в фиолетовый (аметист),
золотистый (цитрин), дымчатый (раухтопаз) и черный (морион) цвета. Такая окраска зависит от посторонних примесей. Если разрезать длинный кристалл турмалина вдоль
оси, то он окажется послойно окрашенным в самые разнообразные цвета: розовые,
зеленые, голубые, бурые, черные.
Цветом
черты минерала называется цвет следа, остающегося на матовой шероховатой поверхности фарфоровой
пластинки, оцарапанной каким-нибудь
минералом. Обычно цвет черты совпадает с цветом самого минерала. Но иногда между ними наблюдается
резкое отличие. Например, черный
гематит имеет красную черту, а соломенно-желтый пирит - черную.
Спайность
- это свойство минералов раскалываться по ровным плоскостям в определенных кристаллографических
направлениях. Оно обусловлено строением кристаллической решетки минералов.
Различают следующие виды
спайности: весьма совершенную, совершенную, среднюю и несовершенную. Весьма совершенной спайностью
обладают такие минералы, как слюды, хлорит и др. Их кристаллы легко
расщепляются. Кристаллы кальцита,
флюорита, полевого шпата имеют совершенную спайность. Они раскалываются, образуя гладкие блестящие поверхности. На обломках минералов, обладающих средней
спайностью (например, пироксенов), наряду с
неровными поверхностями отчетливо видны и гладкие
блестящие поверхности. В случае несовершенной спайности зерна минералов ограничены неправильными
поверхностями, за исключением
граней кристаллов (например, кварц, пирит). Число плоскостей спайности зависит от симметрии (сингонни) кристалла.
Так, у сфалерита (кубическая
сннгония) имеется шесть разно ориентированных плоскостей спайности. Минералы
низших сингонии имеют спайность только в одном направлении. Например, весьма совершенная спайность слюды мусковита. Минералы с хорошей спайностью, легко
раскалывающиеся на пластины, называются «шпатами» (термин шведского
происхождения).
Твердость
минералов обусловлена прочностью их кристаллической решетки. Одним из распространенных способов
определения относительной
твердости минералов является царапание исследуемого минерала острыми краями эталонных минералов «шкалы
Мооса». Эта десятибалльная
шкала предложена в 1811г. немецким ученым Ф. Моосом. Твердость эталонных
минералов в ней соответствует их номерам (табл.
3).
Таблица 3
Относительная твердость минералов в шкале
Мооса
|
Минерал |
Твердость |
|
Тальк |
1 |
|
Гипс |
2 |
|
Кальцит |
3 |
|
Флюорит |
4 |
|
Апатит |
5 |
|
Ортоклаз |
6 |
|
Кварц |
7 |
|
Топаз |
8 |
|
Корунд |
9 |
|
алмаз |
10 |
Если
эталонный минерал оставляет царапину на поверхности исследуемого минерала, то твердость последнего
меньше твердости эталонного минерала.
Плотность.
По плотности (массе единичного объема вещества) минералы подразделяются на легкие (до 2500 кг/м3),
средние (2500-4000 кг/м3),
тяжелые (4000-8000 кг/м3) и весьма тяжелые (более 8000 кг/м3).