ТЕМА 9. ГЕМОГЛОБИН И
ХИМИЯ ДЫХАНИЯ
Содержание
темы.
Гемоглобин. Строение гема и глобина. Различные формы гемоглобина.
Гетерогенность гемоглобина. Спектральные характеристики гемоглобина. Содержание
гемоглобина в крови. Анемии. Перенос кислорода кровью. Кислородная емкость
крови. Кривая диссоциации оксигемоглобина. Артериовенозная разница по кислороду.
Различные формы гипоксии.
Перенос углекислого газа кровью от
тканей к легким. Образование угольной кислоты. Карбоангидраза. Хлоридный сдвиг.
Карбогемоглобин.
Вопросы для обсуждения
1. Строение гемоглобина и
миоглобина. Сравнительная характеристика структуры и свойств этих белков.
2. Функции, производные и
аномальные формы гемоглобина.
3. Пути использования О2
в клетках, пути образования СО2 в клетках, происхождение биохимических
компонентов плазмы крови.
4. Общий анализ крови, ацидоз и
алкалоз.
Тестовые задания для самоконтроля
|
1 |
Молекула гемоглобина состоит из следующего количества
полипептидных цепей 1. Одной 2. Четырёх 3. Трёх 4. Двух |
|
2 |
В центре гема располагается следующий ион 1. Fe3+ 2. Cu+ 3. Fe2+ 4. Cu2+ |
|
3 |
Окисленный гемоглобин, содержащий гематин, называется 1. Дезоксигемоглобином 2. Метгемоглобином 3. Карбаминогемоглобином 4. Оксигемоглобином |
|
4 |
Белковый компонент гемоглобина называется 1. Альбумином 2. Вердоглобином 3. Глобином 4. Глобулином |
|
5 |
В состав гемоглобина взрослого человека
(HbA) входят
следующие субъединицы 1. g 2. ζ 3. a 4. b |
|
6 |
В состав гемоглобина плода (HbF) входят следующие субъединицы 1.
a 2.
b 3.
g 4. ζ |
|
7 |
В видимой области спектра оксигемоглобин
имеет максимум поглощения при следующей длине волны 1. 540 нм 2. 450 нм 3. 590 нм 5. 650 нм |
|
8 |
Установите соответствие между
формами гемоглобина и их названиями 1. Hb 2. HbО2 3. HbNO 4. MetHb A.
Метгемоглобин Б. Оксигемоглобин В. Дезоксигемоглобин,
восстановленный гемоглобин Г. Нитрогемоглобин |
|
9 |
В эритроцитах плода большую часть
гемоглобина составляет 1. HbА 2. HbС 3. HbF 4. HbS |
|
10 |
Среднее содержание гемоглобина (в
г/л) в крови у мужчин составляет 1. 140 2. 200 3. 158 4. 110 |
|
11 |
Среднее содержание гемоглобина (в г/л)
в крови у женщин составляет 1. 140 2. 158 3. 200 4. 110 |
|
12 |
Кислородная ёмкость крови у
взрослого человека составляет 2. 3. 4. |
|
13 |
Установите соответствие между формой углекислого газа и количеством
в крови 1. В виде HCO3-
в плазме 2. В связанном с гемоглобином виде (образуя карбаминовую
связь) 3. В виде бикарбонатов в
эритроците A. 35% B. 10% С. 45% |
|
14 |
Фермент, ускоряющий гидратацию молекулы
углекислого газа с образованием угольной кислоты, называется 1. Дегидратаза 2. Гидроксилаза 3. Карбоангидраза 4. Аминотрансфераза |
|
15 |
Расположите события, происходящие
при переносе углекислого газа, в правильной последовательности 1. Диссоциация слабой кислоты на ионы бикарбоната и
водорода 2. Выход ионов бикарбоната из эритроцита 3. Углекислый газ переносится по градиенту напряжения из
тканей в капилляры 4. В эритроцитах происходит гидратация молекулы СО2
с образованием угольной кислоты |
Лабораторная работа №20
Определение концентрации
гемоглобина в крови
унифицированным колориметрическим
методом
Принцип
метода. Под действием феррицианида калия гемоглобин
окисляется в метгемоглобин (гемиглобин), который в присутствии ацетонциангидрина
трансформируется в окрашенный комплекс цианометгемиглобин (гемиглобинцианид),
интенсивность окраски которого пропорциональна концентрации гемоглобина в крови
и определяется фотометрически при длине волны 540 (520-560) нм.
Исследуемый
материал. Свежая капиллярная кровь. Внимание, кровь берется из
пальца специалистом, имеющим право на эту процедуру, с использованием
стерильных скарификаторов и с соблюдением мер предосторожности.
Состав
набора.
1. Монореагент, концентрат (20 мл).
2. Калибратор (калибровочный
раствор гемоглобина с концентрацией 120 г/л).
Подготовка
реагентов к процедуре анализа и их стабильность. Рабочий
реагент: перед проведением анализа смешайте необходимое количество монореагента
с дистиллированной водой в соотношении 1:9. Рабочий реагент можно хранить в
темном месте в плотно закрытом флаконе при комнатной температуре (+18-25°С) не
более 2 месяцев. Монореагент после вскрытия флаконов стабилен в течение всего
срока годности при хранении при комнатной температуре (+18-25°С). Калибратор
после вскрытия флакона стабилен не менее 3-х месяцев при условии достаточной
герметизации флакона и хранении в защищенном от света месте при +2-8°С. Не
замораживать.
Ход работы
Для определения концентрации
гемоглобина подготовьте пробы в соответствии с табл. 20.
Таблица 20
|
Состав
проб |
Опытная
проба |
Калибровочная
проба |
Контрольная
проба |
|
Рабочий реагент, мл |
5,00 |
5,00 |
5,00 |
|
Кровь, мл |
0,02 |
– |
– |
|
Калибратор, мл |
– |
0,02 |
– |
|
Вода дистиллированная, мл |
– |
– |
0,02 |
Объемы исследуемого образца можно
изменить, соблюдая соотношение 1:250.
После забора крови оботрите
пипетку, кровь внесите в пробирку, содержащую рабочий реагент, и несколько раз
промойте пипетку в этом растворе. Содержимое пробирок тщательно перемешайте. Через
3-5 мин измерьте оптическую плотность опытных и калибровочной проб против
рабочего реагента в кювете с длиной оптического пути 1 см при длине волны 540
(520-560) нм. Окраска стабильна в течение 6-ти часов в защищенном от света
месте.
Расчет.
Концентрацию
гемоглобина в исследуемом образце (С, г/л) рассчитайте по формуле:
![]() ,
,
где Е пробы – оптическая плотность опытной пробы, Е калибратора –
оптическая плотность калибровочной пробы, 120 – концентрация гемоглобина в калибраторе,
г/л.
Нормальные
значения: мужчины: 132-164 г/л; женщины: 115-145 г/л.
ЗАДАНИЕ
1. Определите содержание
гемоглобина в собственной крови.
2. Проведите сравнительный анализ
содержания гемоглобина в крови у студентов в группе и сделайте вывод.
|
|
|
|
|
|
|
|
Лабораторная работа №21
Количественное определение
концентрации общего
и прямого билирубина в сыворотке
крови
Принцип
метода. Прямой билирубин непосредственно реагирует с
диазотированной сульфаниловой кислотой, а общий билирубин – в присутствии
кофеинового реагента, образуя окрашенное азосоединение, интенсивность окраски
которого пропорциональна содержанию билирубина; измеряется фотометрически при
длине волны 535 (500-560) нм.
Исследуемый
материал. Свежая негемолизированная сыворотка крови.
Состав
набора.
1. Кофеиновый реагент.
2. Сульфаниловая кислота.
3. Натрия нитрит.
4. Физиологический раствор.
5. Калибратор (лиофилизат), концентрация
билирубина после растворения содержимого в 1 мл деионизованной воды – 171
мкмоль/л.
Подготовка
реагентов к процедуре анализа и их стабильность.
Приготовление рабочего реагента. Смешайте необходимые
количества сульфаниловой кислоты и натрия нитрита в соотношении 40:1.
Полученный рабочий реагент (диазореагент) стабилен в течение 10 дней при +2-8°С
в плотно закрытой посуде из темного стекла или не менее 48 часов при +18-25°С.
Приготовление калибратора. Содержимое флакона с
лиофилизатом калибратора растворите в 1,0 мл деионизованной воды. Концентрация
билирубина в полученном растворе калибратора составляет 171 мкмоль/л.
Приготовленный калибратор стабилен в защищенном от света месте при +2-8°С не
более 5 дней.
Ход анализа
Приготовьте пробы в соответствии с
табл. 21:
Таблица 21
|
Состав проб |
Опытные пробы |
Контрольная проба |
Калибровочная проба |
|
|
общий билирубин |
прямой билирубин |
|||
|
Сыворотка крови, мл |
0,4 |
0,4 |
0,4 |
– |
|
Калибратор, мл |
– |
– |
– |
0,4 |
|
Физ. раствор, мл |
0,4 |
3,2 |
3,6 |
0,4 |
|
Кофеиновый реагент,
мл |
2,8 |
– |
– |
2,8 |
|
Рабочий реагент, мл |
0,4 |
0,4 |
– |
0,4 |
Пробы
тщательно перемешайте. Для определения прямого билирубина пробу фотометрируйте
не позднее 5 мин после добавления рабочего реагента. Для определения общего
билирубина пробу инкубируйте при +18-25°С в течение 20 мин. Оптическую
плотность опытных проб измерьте против контрольной (холостой) пробы при длине
волны 535 (500-560) нм в кювете с длиной оптического пути 1,0 см. Оптическую
плотность калибратора измерьте в тех же условиях против дистиллированной воды.
Расчет
концентрации (С, мкмоль/л) билирубина в исследуемом
образце проведите по формуле:
![]() ,
,
где С – концентрация билирубина в
мкмоль/л; Е пробы – оптическая
плотность опытной пробы; Е калибратора
– оптическая плотность калибровочной пробы; 171 мкмоль/л – концентрация
билирубина в калибраторе.
Нормальные показатели: прямого
билирубина – до 4 мкмоль/л; общего билирубина – 8,5-20,5 мкмоль/л.
ЗАДАНИЕ
1. Определите содержание билирубина
в сыворотке крови человека и крысы.
2. Сделайте вывод.
|
|
|
|
|
|
|
|
Лабораторная работа №22
Изучение оптических свойств
различных форм гемоглобина
Каждая форма гемоглобина
характеризуется определенным спектром поглощения, представляющим собой зависимость
оптической плотности раствора гемоглобина от длины волны света. Наиболее
интенсивной полосой в спектре поглощения гемоглобина является полоса Соре, принадлежащая
порфириновой части его молекулы (рис. 5).
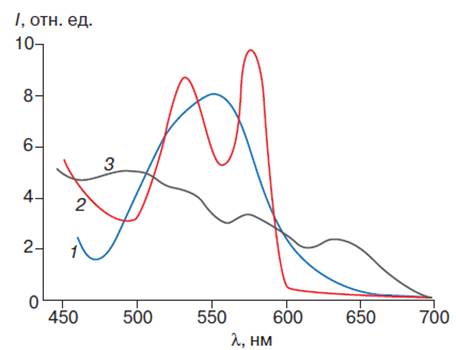
Рис. 5. Спектр поглощения
производных гемоглобина. Спектры поглощения дезоксигемоглобина (1),
оксигемоглобина (2) и ферригемоглобина (3)
По изменению положения и
интенсивности поглощения этой полосы можно судить о структурных изменениях
молекул различных форм гемоглобина (табл. 22).
Таблица 22
Спектральные характеристики различных форм
гемоглобина
|
Формы гемоглобина |
α-Полоса |
β-Полоса |
Полоса
Соре |
|||
|
λ,
нм |
ελ,
М-1см-1 |
λ,
нм |
ελ,
М-1см-1 |
λ,
нм |
ελ,
М-1см-1 |
|
|
Оксигемоглобин |
557 |
14600 |
542 |
13800 |
412 |
135000 |
|
Дезоксигемоглобин |
555 |
13500 |
|
|
430 |
119000 |
|
Карбоксигемоголобин |
569 |
13400 |
539 |
13400 |
419 |
191000 |
Оборудование
и материалы. СФ-(46) или другой спектрофотометр,
центрифуга на 9000 об/мин, центрифужные пробирки, кюветы, пенициллиновые
флаконы, пипетки Пастера, прибор для получения оксида углерода, гемоглобин кристаллический,
хлористый натрий, гепарин, бихромат калия, феррицианид калия, дитионит натрия.
Получение
раствора оксигемоглобина. Для работы рекомендуется использовать
свежеприготовленные растворы гемоглобина. Кровь берут у декапитированных животных.
Цельную кровь стабилизируют гепарином, растворенным в 0,85%-ном растворе
хлористого натрия. Для отделения плазмы стабилизированную кровь центрифугируйте
в течение 10 мин при 3000 об/мин. Плазму крови отберите пипеткой. К эритроцитам
добавьте трехкратный объем 0,85%-ного раствора хлористого натрия, осторожно при
этом размешивая суспензию стеклянной палочкой. Суспензию центрифугируйте в течение
5 мин при 6000 об/мин. Промойте эритроциты 3 раза. Промытые эритроциты
подвергните гемолизу дистиллированной водой в течение 20 мин. Стромы осадите центрифугированием
при 9000 об/мин в течение 15 мин. В прозрачном гемолизате определите содержание
гемоглобина с помощью приведенного в работе № 20 метода.
Ход
анализа
Регистрация
спектра поглощения оксигемоглобина. Раствор
оксигемоглобина разбавьте дистиллированной водой до оптической плотности
раствора, попадающей в диапазон 0,4-0,5. Снимите спектр поглощения раствора
оксигемоглобина в интервале длин волн 380-600 нм (оптическая плотность раствора
измеряется через каждые 5 нм).
Регистрация
спектра поглощения метгемоглобина. Добавьте к раствору
оксигемоглобина 1-2 капли насыщенного раствора феррицианида калия. Визуально
оцените изменение окраски. Раствор метгемоглобина имеет коричневую окраску.
Снимите спектр поглощения раствора гемоглобина в интервале длин волн 380-600
нм. Для компенсации светопоглощения за счет феррицианида в контроль добавьте
такой же объем раствора этого вещества, какой был добавлен к раствору
оксигемоглобина.
Регистрация
спектра поглощения метгемоглобина. Добавьте к водному
раствору оксигемоглобина несколько кристаллов дитионита натрия (Na2S2O4).
Визуально оцените изменение окраски. Ярко алая окраска (цвет оксигемоглобина)
переходит в синевато-красную, характерную для гемоглобина. Снимите спектр
поглощения раствора в интервале длин волн 380-600 нм.
ЗАДАНИЕ
1. Представьте в графическом виде
зависимость оптической плотности различных состояний гемоглобина от длины
поглощаемого света (спектр поглощения), откладывая по оси ординат оптическую
плотность раствора, а по оси абсцисс соответствующие длины волн.
2. Найдите минимумы и максимумы
поглощения гемоглобинов и сделайте вывод.
|
|
|
|
|
|
|
|