ТЕМА 3. ЛИПИДЫ ПЛАЗМЫ КРОВИ
Содержание темы. Общая характеристика липидов
плазмы. Липопротеиды плазмы крови. Общая характеристика липопротеидов.
Физиологическая роль липопротеидов. Строение липопротеидной частицы.
Классификация липопротеидов по гидратированной плотности, скорости флотации,
электрофоретической подвижности, различиям в апопротеиновом составе.
Характеристика
различных классов липопротеидов. Липопротеиды, богатые триглицеридами.
Хиломикроны и липопротеиды очень низкой плотности: состав, содержание в плазме,
образование и элиминация. Липопротеиды, богатые холестерином. Липопротеиды
низкой плотности. Липопротеиды, богатые фосфолипидами. Липопротеиды высокой
плотности: состав, роль, образование и катаболизм.
Вопросы для обсуждения
1. Общая
характеристика липидного состава плазмы крови.
2. Транспорт липидов.
Механизмы транспорта липидов в сыворотке крови. Липопротеиды плазмы крови:
классификация.
3. Строение
липопротеидной частицы, виды и функции апопротеинов.
4. Общие пути синтеза
липопротеинов. Характеристика, метаболизм, функции основных классов
липопротеидов.
5. Ассимиляция липидов тканями, роль
липопротеинлипазы и рецепторов.
6.
Дислипопротеинемии.
7. Гиперлипопротеинемии:
понятие, классификация, причины. Изменения липидного состава плазмы крови при
различных формах гиперлипопротеинемий.
8. Модифицированные
липопротеиды: понятие, механизмы модификации, особенности метаболизма, роль в
развитии атеросклероза.
9. Диагностическое
значение определения ЛПНП и ЛПВП в плазме крови.
Тестовые задания для самоконтроля
|
1 |
Суммарное содержание липидов в
плазме крови здоровых взрослых людей составляет 1. 5-10 г/л 2. 10-12 г/л 3. 4-8 г/л 4. 2-6 г/л |
|
2 |
Содержание триглицеридов в плазме
крови взрослых людей составляет 1. 1,5-2,5 г/л 2. 0,5-1,9 г/л 3. 0,3-0,6 г/л 4. 1,1-2,8 г/л |
|
3 |
Содержание неэстерифицированных
жирных кислот (НЭЖК) в плазме крови взрослых людей составляет 1. 0,08-0,2 г/л 2. 0,5-1,9 г/л 3. 0,3-0,6 г/л 4. 0,06-0,09 г/л |
|
4 |
Общее содержание холестерина в плазме крови здоровых
взрослых людей составляет 1. 0,5-1,9 г/л 2. 0,3-0,6 г/л 3. 1,1-2,8 г/л 4. 1,5-2,5 г/л |
|
5 |
В состав поверхностного слоя
(оболочки) липопротеиновой частицы входят следующие липиды 1. Неэстерифицированный холестерин 2. Эстерифицированный холестерин 3. Триацилглицеролы 4. Фосфолипиды |
|
6 |
В состав ядра липопротеиновой
частицы входят следующие липиды 1. Триацилглицеролы 2. Неэстерифицированный холестерин 3. Эстерифицированный холестерин 4. Фосфолипиды |
|
7 |
Установите соответствие между
типом липопротеидов и плотностью солевых растворов для их выделения 1. Хиломикроны 2. ЛПОНП 3. ЛПНП 4. ЛППП 5. ЛПВП A. 1,019-1,063 Б. < 0,95 В. 0,95-1,006 Г. 1,006-1,019 Д. 1,063-1,210 |
|
8 |
Расположите в правильной
последовательности липопротеины при электрофорезе, начиная со старта 1. Пре-β-липопротеины (ЛПОНП) 2. α-Липопротеины (ЛПВП) 3. Хиломикроны 4. β-Липопротеины (ЛПНП) |
|
9 |
Установите соответствие между
классом липопротеинов и их химическим составом 1. Хиломикроны 2. ЛПОНП 3. ЛПНП 4. ЛПВП A. Около 50% эфиров холестерина и холестерина 20% белка Б. Около 5-12% белков и 50-70%
триацилглицеринов В. Около 90% триацилглицеринов и 2%
белков Г. Около 50% белков и 20% эфиров холестерина и холестерина |
|
10 |
Установите соответствие между
классом липопротеидов и соответствующим названием по электрофоретической
подвижности 1. Хиломикроны 2. ЛПОНП 3. ЛПНП 4. ЛПВП A. b-ЛП Б. Остаются на старте В. a-ЛП Г. Пре-b-ЛП |
|
11 |
Установите соответствие между
классом липопротеинов и местом их образования в организме человека 1. Хиломикроны 2. ЛПОНП 3. ЛПНП 4. ЛПВП-предшественники A. Печень Б. Кровь В. Слизистая тонкого кишечника Г. Печень и слизистая тонкого
кишечника |
|
12 |
Содержание хиломикронов в плазме
крови взрослых лиц натощак составляет 1. 0,5-2,0 г/л 2. Следы 3. 2-3 г/л 4. 0,1-0,5 г/л |
|
13 |
ЛПОНП участвуют в транспорте
следующих липидов 1. Свободных жирных кислот 2. Экзогенных триглицеридов 3. Эндогенных триглицеридов 4. Фосфолипидов |
|
14 |
Содержание ЛПНП2 в
плазме крови взрослых лиц натощак составляет 1. 2-3 г/л 2. 0,5-2,0 г/л 3. 0,1-0,5 г/л 4. Следы |
|
15 |
Роль ЛПВП в организме заключается
в следующем 1. Транспортируют ионы металлов 2.Транспортируют свободные жирные кислоты 3. Поддерживают гомеостаз холестерина плазмы крови и
тканей 4. Формируют систему комплемента |
Лабораторная работа №5
Колориметрический метод определения
общих липидов в сыворотке и плазме крови
Принцип
метода. Продукты распада ненасыщенных липидов образуют с реактивом,
состоящим из серной и фосфорной кислот и ванилина, соединение, интенсивность
окраски которого прямо пропорциональна концентрации общих липидов в пробе.
Исследуемый
материал. Сыворотка или плазма. Общие липиды в пробе стабильны
23 часа при комнатной температуре (15-25°С) или 3 дня при 2-8°С.
Состав
набора.
1. Реагент 1 (фосфованилин, 235 ммоль/л).
2. Стандарт (общие липиды, хлороформенный
раствор триолеина, 7,5 г/л).
3. Дополнительный реагент (серная кислота)
не входит в набор.
Подготовка
реагентов к процедуре анализа и их стабильность. Реагент
и стандарт готовы к использованию.
Ход анализа
К 0,1 мл сыворотки крови, стандартного
раствора липидов или дистиллированной воды прибавьте 2,5 мл серной кислоты как
указано в табл. 4.
Таблица 4
|
Состав проб |
Опытная проба |
Калибровочная проба |
Контрольная проба |
|
Проба, мл |
0,1 |
– |
– |
|
Стандарт, мл |
– |
0,1 |
– |
|
Вода, мл |
– |
– |
0,1 |
|
Серная кислота, мл |
2,5 |
2,5 |
2,5 |
Пробы тщательно перемешайте и поместите
в кипящую водяную баню на 10 мин. После этого пробы охладите водопроводной
водой. Из каждой пробы отберите 0,2 мл смеси и перенесите в другие пробирки, содержащие
3 мл Реагента 1 (фосфованилин) как указано в табл. 5.
Таблица 5
|
Состав пробы |
Опытная проба |
Калибровочная проба |
Контрольная проба |
|
Надосадочная жидкость, мл |
0,2 |
0,2 мл |
0,2 мл |
|
Реагент 1, мл |
3,0 мл |
3,0 мл |
3,0 мл |
После
тщательного перемешивания пробы оставьте на 45 мин в темноте при комнатной
температуре или инкубируйте при 37°С в течение 15 мин. Оптическую плотность
пробы и стандарта измерьте при 520 (490-550) нм против контрольной пробы в
кювете на 0,5 см. Окраска стабильна до 1 часа.
Расчет.
Концентрацию общих липидов в плазме или сыворотке (С, г/л) рассчитайте по
формуле:

где С – концентрация общих липидов
в г/л, Е пробы – оптическая плотность
опытной пробы, Е стандарта –
оптическая плотность стандартной пробы, 7,5 – концентрация общих липидов в
стандарте.
Нормальные
значения. Концентрация общих липидов в сыворотке и в плазме крови
составляет 4,5-8,0 г/л.
ЗАДАНИЕ
1. Определите содержание общих липидов
в сыворотке (плазме) крови.
2. Сделайте вывод.
|
|
|
|
|
|
|
|
|
|
Лабораторная работа №6
Количественное определение
содержания триглицеридов в крови
Принцип
метода. Определение концентрации триглицеридов основано на проведении
ряда сопряжённых ферментативных реакций, катализируемых липазой, глицерокиназой
(ГК) в присутствии АТФ, глицеролфосфатоксидазой (ГФО) и пероксидазой (ПО).
Образующаяся в ходе данных реакций
перекись водорода (Н2О2) способствует окислительному азосочетанию
4-аминоантипирина (4-ААП) и фенола с образованием окрашенного соединения (хинониминовый
краситель).
Интенсивность окраски реакционной
среды пропорциональна содержанию триглицеридов в исследуемом материале и измеряется
фотометрически при длине волны 500 (490-520) нм.
 Схема
реакции:
Схема
реакции:
Исследуемый
материал. Свежая негемолизированная сыворотка, ЭДТА- или
гепаринизированная плазма крови. Билирубин в концентрации до 300 мкмоль/л и гемоглобин
в концентрации до 6,0 г/л не влияют на правильность определения триглицеридов.
Состав
набора. Реагент 1. Реагент 2. Калибратор (калибровочный
раствор триглицеридов с концентрацией 2,29 ммоль/л в пересчете на триолеин).
Подготовка
реагентов к процедуре анализа и их стабильность. Приготовление
рабочего реагента: содержимое одного флакона с Реагентом 2 растворите в содержимом
одного флакона с Реагентом 1 при аккуратном перемешивании. Рабочий реагент
готов к применению через 20 минут после полного растворения лиофилизата. Рабочий
реагент храните при +2-8°С в защищённом от света месте в плотно закрытом
флаконе не более 20 дней.
Тщательно закрывайте флаконы с реагентами
после каждого использования!
Ход анализа
Внесите в пробирки рабочий реагент,
анализируемые образцы, калибратор и дистиллированную воду в объёмах, указанных
в табл. 6.
Таблица 6
|
Состав проб |
Опытная проба |
Калибровочная проба |
Контрольная проба |
|
Рабочий реагент, мл |
2,00 |
2,00 |
2,00 |
|
Исследуемый образец,
мл |
0,02 |
– |
– |
|
Калибратор, мл |
– |
0,02 |
– |
|
Вода
дистиллированная, мл |
– |
– |
0,02 |
Реакционную смесь тщательно перемешайте
и инкубируйте в течение 15 мин при комнатной температуре (+18-25°С) или в течение
10 минут при +37°С. Измерьте оптическую плотность опытной и калибровочной проб
против контрольной (холостой) пробы при длине волны 500 (490-520) нм в кювете с
длиной оптического пути 1,0 см.
Окраска растворов стабильна в течение
2 часов после окончания инкубации при хранении проб в защищённом от света месте
при комнатной температуре (+18-25°С).
Расчет
концентрации триглицеридов в исследуемом образце
произведите по следующей формуле:
 ,
,
где С – концентрация триглицеридов
в моль/л, Е пробы – оптическая плотность
опытной пробы, Е калибратора – оптическая
плотность калибровочной пробы, 2,29 – концентрация триглицеридов в калибраторе,
ммоль/л.
Нормальные
показатели. Концентрация триглицеридов в сыворотке или
плазме крови в норме составляет 0,34-1,71 ммоль/л.
ЗАДАНИЕ
1. Определите содержание триглицеридов
в сыворотке (плазме) крови крыс.
2. Сделайте вывод.
|
|
|
|
|
|
|
|
|
|
Лабораторная работа №7
Определение содержания общего холестерина
в сыворотке (плазме) крови
Принцип
метода. Холестерин из состава эфиров высвобождается под действием
фермента холестеролэстеразы (ХЭ). При участии фермента холестеролоксидазы (ХО)
холестерин окисляется до 4-холестен-3-она. Образующаяся перекись водорода при
участии фермента пероксидазы (ПО) способствует окислительному азосочетанию
4-аминоантипирина (4-ААП) и фенола с образованием окрашенного соединения (хинониминовый
краситель). Интенсивность окраски реакционной среды пропорциональна содержанию
холестерина в исследуемом материале и определяется фотометрически при длине
волны 500 (490-520) нм.
 Схема реакции:
Схема реакции:

Концентрация хинонимина, определяемая
фотометрически, пропорциональна концентрации холестерина в пробе.
Исследуемый
материал. Сыворотка, гепаринизированная или ЭДТА-плазма крови
без следов гемолиза. Проба стабильна 7 дней при 2-8°С.
Состав
набора. Монореагент:
Калибратор – раствор холестерина с
концентрацией 5,17 ммоль/л (200 мг/100 мл) (1,5 мл).
Ход анализа
Готовьте инкубационные пробы согласно табл. 7.
Таблица
7
|
Состав проб |
Опытная проба |
Калибровочная проба |
Контрольная проба |
|
Монореагент, мл |
2,0 |
2,0 |
2,0 |
|
Сыворотка (плазма),
мл |
0,02 |
– |
– |
|
Калибратор, мл |
– |
0,02 |
– |
|
Вода
дистиллированная, мл |
– |
– |
0,02 |
Пробы перемешайте и инкубируйте не
менее 15 мин при температуре 18-25°С или 10 минут при 37°С. Измерьте оптическую
плотность опытной и калибровочной проб против контрольной пробы при длине волны
500 нм (490-520 нм). Окраска стабильна не менее 2 часов после окончания инкубации
при предохранении от прямого света.
Расчет
концентрации (С) холестерина в исследуемом образце проведите
по формуле:
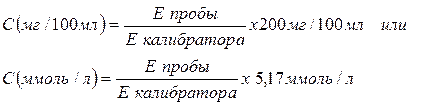
где С – концентрация холестерина в
пробе в моль/л (мг/100 мл); Е пробы –
оптическая плотность опытной пробы, Е калибратора
– оптическая плотность калибровочной пробы, 200 мг/100 мл или 5,17 ммоль/л –
концентрация холестерина в калибраторе.
Нормальные
показатели до 200 мг/100 мл (5,17 ммоль/л);
Пограничные показатели от 200 до
250 мг/100 мл (5,17-6,50 ммоль/л);
Патологические показатели свыше 250
мг/100 мл (6,50 ммоль/л).
ЗАДАНИЕ
1. Определите содержание
холестерина в сыворотке (плазме) крови человека и крысы.
2. Сделайте вывод.
|
|
|
|
|
|
|
|
|
|